 :参照ウィンドウに表示 特許・実用新案 審査基準
:参照ウィンドウに表示 特許・実用新案 審査基準 第2章 生物関連発明
第2章 生物関連発明
この章では、生物関連発明に係る出願の審査に際し、特有な判断・取扱いが必要な事項を中心に説明する。
ここでいう生物は、微生物、植物又は動物を意味し、これには増殖可能な動植物の細胞も含まれる。
 1. 遺伝子工学
1. 遺伝子工学
ここでは、生物関連発明のうち遺伝子工学に関するものを取り扱う。ここでの「遺伝子工学」とは、遺伝子組換え、細胞融合等により人為的に遺伝子を操作する技術を意味する。
遺伝子工学に関する発明には、遺伝子、ベクター、組換えベクター、形質転換体、融合細胞、形質転換技術により得られたタンパク質(以下「組換えタンパク質」と称する。) 、モノクローナル抗体等に関する発明が含まれる。
微生物、植物、動物に関する発明であって、遺伝子工学によって得られたものは、原則としてここにおいて取り扱う。
 1.1 明細書及び特許請求の範囲の記載要件
1.1 明細書及び特許請求の範囲の記載要件
 1.1.1 特許請求の範囲
1.1.1 特許請求の範囲
第36条第6項第2号 の規定は特許を受けようとする発明が明確であることを要件としていることから、特許請求の範囲は、一の請求項から発明が明確に把握されるように記載しなければならない。
の規定は特許を受けようとする発明が明確であることを要件としていることから、特許請求の範囲は、一の請求項から発明が明確に把握されるように記載しなければならない。
したがって、遺伝子、ベクター、組換えベクター、形質転換体、融合細胞、組換えタンパク質、モノクローナル抗体に係る発明においては、請求項は以下のように記載する。
- (1)
-
遺伝子
- ①
-
遺伝子は、塩基配列により特定して記載することができる。
- ②
-
構造遺伝子は、当該遺伝子によってコードされたタンパク質のアミノ酸配列により特定して記載することができる。
例:Met-Asp-・・・・Lys-Gluで表されるアミノ酸配列からなるタンパク質をコードする遺伝子。
- ③
-
遺伝子は、「欠失、置換若しくは付加された」、「ハイブリダイズする」等の表現及び当該遺伝子の機能、更に必要に応じて起源・由来等を組み合わせて以下のような包括的な記載をすることができる(ただし、発明が明確であること、及び、実施可能要件(1.1.2.1 参照)を満たすことが必要である点に留意する。)。
- 例1:
以下の(a)又は(b)のタンパク質をコードする遺伝子。
- (a)
-
Met-Asp-・・・・Lys-Gluのアミノ酸配列からなるタンパク質
- (b)
-
アミノ酸配列(a)において1若しくは数個のアミノ酸が欠失、置換若しくは付加されたアミノ酸配列からなり、かつA酵素活性を有するタンパク質
- (注)
-
(a)のタンパク質はA酵素活性を有するものである。
(b)のタンパク質をコードする遺伝子については、当業者に期待しうる程度を超える試行錯誤や複雑高度な実験を行うことなく当業者が作ることができるように、発明の詳細な説明に記載されているものとする。
- 例2:
以下の(a)又は(b)のDNAからなる遺伝子。
- (a)
-
ATGTATCGG・・・TGCCTの塩基配列からなるDNA
- (b)
-
(a)の塩基配列からなるDNAと相補的な塩基配列からなるDNAとストリンジェントな条件下でハイブリダイズし、かつB酵素活性を有するタンパク質をコードするヒト由来のDNA
- (注)
-
(a)のDNAがコードするタンパク質はB酵素活性を有するものである。
「ストリンジェントな条件」については、発明の詳細な説明に記載されているものとする。
- ④
-
遺伝子は、その機能、理化学的性質、起源・由来、製法等により特定して記載することもできる(ただし、発明が明確であること 、及び、実施可能要件(1.1.2.1参照)を満たすことが必要である点に留意する。)。
- (2)
-
ベクター
ベクターは、DNA塩基配列、開裂地図、分子量、塩基対数、採取源、製法、その機能、性質等により特定して記載することができる。
- (注)
-
開裂地図とは、各種制限酵素による開裂部位の位置関係、距離等を示したものをいう。
- (3)
-
組換えベクター
組換えベクターは、遺伝子とベクターの少なくとも一方を特定して記載することができる。
- 例:
-
ACAGCA・・・・・・AGTCACの塩基配列である遺伝子を含有する組換えベクター。
- (4)
-
形質転換体
形質転換体は、①宿主、②導入遺伝子(又は組換えベクター)、の少なくとも一方を特定して記載することができる(ただし、発明が明確であること、及び、実施可能要件(1.1.2.1参照)を満たすことが必要である点に留意する)。
- 例1:
-
Met-Asp-・・・・Lys-Gluのアミノ酸配列を有するタンパク質をコードする遺伝子を含有する組換えベクターを含む形質転換体。
- 例2:
ATGACT・・・・・・の塩基配列からなる毒素遺伝子が挿入されており、かつ、該毒素遺伝子が発現している植物。
- 例3:
-
乳タンパク質の製造に関与する遺伝子の遺伝子制御領域に任意のタンパク質をコードする構造遺伝子を結合させた組換えDNAを有し、該任意のタンパク質を乳中に分泌することを特徴とする非ヒト哺乳動物。
- (5)
-
融合細胞
融合細胞は、使用した親細胞、融合細胞の機能・性質、融合細胞の製法等により特定して記載することができる。
- (6)
-
組換えタンパク質
- ①
-
組換えタンパク質は、アミノ酸配列又は該アミノ酸配列をコードする構造遺伝子の塩基配列により特定して記載することができる。
- 例:
-
Met-Tyr-・・・・Cys-Leuで表されるアミノ酸配列からなる組換えタンパク質。
- ②
-
組換えタンパク質は、「欠失、置換若しくは付加された」等の表現及び当該組換えタンパク質の機能、更に必要に応じて当該組換えタンパク質をコードする遺伝子の起源・由来等を組み合わせて以下のような包括的な記載をすることができる(ただし、発明が明確であること、及び、実施可能要件(1.1.2.1参照)を満たすことが必要である点に留意する。)。
- 例:
-
以下の(a)又は(b)の組換えタンパク質。
- (a)
-
Met-Tyr-・・・・Cys-Leuで表されるアミノ酸配列からなるタンパク質
- (b)
-
アミノ酸配列(a)において1若しくは数個のアミノ酸が欠失、置換若しくは付加されたアミノ酸配列からなり、かつA酵素活性を有するタンパク質
- (注)
-
(a)のタンパク質はA酵素活性を有するものである。
(b)のタンパク質については、当業者に期待しうる程度を超える試行錯誤や複雑高度な実験を行うことなく当業者が作ることができるように、発明の詳細な説明に記載されているものとする。
- ③
-
組換えタンパク質は、その機能、理化学的性質、起源・由来、製法等により特定して記載することもできる(ただし、発明が明確であること、及び、実施可能要件(1.1.2.1参照)を満たすことが必要である点に留意する)。
- (7)
-
モノクローナル抗体
モノクローナル抗体は、モノクローナル抗体が認識する抗原、モノクローナル抗体を産生するハイブリドーマ、交差反応性等により特定して記載することができる。
- 例1:
-
抗原Aに対するモノクローナル抗体。
- (注)
-
抗原Aは物質として特定して記載されている必要がある。
- 例2:
-
受託番号がATCC HB-○○○○であるハイブリドーマにより産生される、抗原Aに対するモノクローナル抗体。
- (注)
-
抗原Aは物質として特定して記載されている必要がある。
- 例3:
-
抗原Aに反応し、抗原Bに反応しないモノクローナル抗体。
- (注)
-
抗原A及び抗原Bは物質として特定して記載されている必要がある。
 1.1.2 発明の詳細な説明
1.1.2 発明の詳細な説明
発明の詳細な説明は、当業者がその実施をすることができる程度に明確かつ十分に記載しなければならず(実施可能要件)、かつ、発明が解決しようとする課題及びその解決手段その他の当業者が発明の技術上の意義を理解するために必要な事項を記載しなければならない(委任省令要件)。
発明の詳細な説明の記載が上記要件を満たしていない場合には、第36条第4項第1号 違反となる。
違反となる。
 1.1.2.1 実施可能要件
1.1.2.1 実施可能要件
第36条第4項第1号 は「発明の詳細な説明は、・・・その発明の属する技術の分野における通常の知識を有する者がその実施をすることができる程度に明確かつ十分に、記載しなければならない。」と規定されているが、これは、「その発明の属する技術分野において研究開発(文献解析、実験、分析、製造等を含む。)のための通常の技術的手段を用い、通常の創作能力を発揮できる者(当業者)が、明細書及び図面に記載した事項と出願時の技術常識とに基づき、請求項に係る発明を実施することができる程度に、発明の詳細な説明を記載しなければならない」旨を意味するものである。
は「発明の詳細な説明は、・・・その発明の属する技術の分野における通常の知識を有する者がその実施をすることができる程度に明確かつ十分に、記載しなければならない。」と規定されているが、これは、「その発明の属する技術分野において研究開発(文献解析、実験、分析、製造等を含む。)のための通常の技術的手段を用い、通常の創作能力を発揮できる者(当業者)が、明細書及び図面に記載した事項と出願時の技術常識とに基づき、請求項に係る発明を実施することができる程度に、発明の詳細な説明を記載しなければならない」旨を意味するものである。
したがって、明細書及び図面に記載された発明の実施についての教示と出願時の技術常識とに基づいて、当業者が発明を実施しようとした場合に、どのように実施するかが理解できないとき(例えば、どのように実施するかを発見するために、当業者に期待しうる程度を超える試行錯誤や複雑高度な実験等を行う必要があるとき)には、当業者が実施することができる程度に発明の詳細な説明が記載されていないことになる。
- (1)
-
物の発明について
物の発明についての「実施をすることができる」とは、その物を作ることができ、かつ、その物を使用できることであるから、「発明の実施の形態」もこれらが可能となるように記載する必要がある。
また、発明の詳細な説明において、当該「物の発明」について明確に説明されていることが必要である。
したがって、遺伝子、ベクター、組換えベクター、形質転換体、融合細胞、組換えタンパク質、モノクローナル抗体等の発明においては、以下のように記載する。
- ①
-
発明に係る物について明確に説明されていること
この要件を満たすためには、当業者にとって一の請求項から発明が把握でき、その発明が発明の詳細な説明の記載から読み取れればよい。
- ②
-
作ることができること
遺伝子、ベクター、組換えベクター、形質転換体、融合細胞、組換えタンパク質、モノクローナル抗体等の発明においては、当業者がその物を製造することができるように記載しなければならない。このためには、どのように作るかについての具体的な記載がなくても明細書及び図面の記載並びに出願時の技術常識に基づき当業者がそれらの物を製造できる場合を除き、それらの製造方法を具体的に記載しなければならない。
- (ⅰ)
-
遺伝子、ベクター又は組換えベクター
これらの製造方法としては、各々の起源・由来、使用するベクター等の入手手段、使用酵素、処理条件、採取・精製工程、確認手段等を記載する。
請求項において遺伝子が包括的に記載されている場合(1.1.1(1)参照)、それらの遺伝子を得るために、当業者に期待しうる程度を超える試行錯誤や複雑高度な実験等を行う必要があるときには、当業者がその物を作ることができるように発明の詳細な説明が記載されていないことになる。
例えば、実際に取得された遺伝子、及び、これに対し著しく相同性が低い遺伝子を含み、かつ機能により特定されている請求項において、著しく相同性が低い遺伝子の中に、実際に取得された遺伝子と同一の機能を有しない遺伝子が多数含まれることになる場合には、それらの遺伝子の中から、取得された遺伝子と同一の機能を有するものを選択するためには、通常、当業者に期待しうる程度を超える試行錯誤や複雑高度な実験等を行う必要があるので、当業者がその物を作ることができるように発明の詳細な説明が記載されていないことになる。
- 例:
-
以下の(a)又は(b)のDNAからなる遺伝子。
- (a)
-
ATGTATCGG・・・TGCCTの塩基配列からなるDNA
- (b)
-
(a)の塩基配列からなるDNAと相同性が○○%以上の塩基配列からなり、かつB酵素活性を有するタンパク質をコードするDNA
- (注)
-
(a)のDNAがコードするタンパク質はB酵素活性を有するものである。
○○%は、著しく相同性が低い値である。
- (説明)
(b)は機能により特定されているものの、実際に取得された遺伝子(a)に対し著しく相同性が低い遺伝子を含む。「(a)の塩基配列からなるDNAと相同性が○○%以上の塩基配列からなるDNA」の中にB酵素活性を有しないタンパク質をコードするDNAが多数含まれる場合、その中からB酵素活性を有するタンパク質をコードするDNAを選択することは、通常、当業者に期待しうる程度を超える試行錯誤や複雑高度な実験等を行う必要があり、当業者がその物を作ることができるように発明の詳細な説明が記載されていないことになる。
- (ⅱ)
-
形質転換体
形質転換体の製造方法としては、導入される遺伝子又は組換えベクター、宿主(微生物、植物、動物)、遺伝子の導入方法、組換えベクターの導入方法、形質転換体の選択採取方法、確認手段等を記載する。
請求項において形質転換体が包括的な分類学上の単位(例:形質転換された植物、形質転換された非ヒト脊椎動物、形質転換体(微生物、植物、動物を含む。))のものである場合において、それらの形質転換体を得るために、当業者に期待しうる程度を超える試行錯誤や複雑高度な実験等を行う必要があるときには、当業者がその物を作ることができるように発明の詳細な説明が記載されていないことになる。
- (ⅲ)
-
融合細胞
融合細胞の製造方法としては、親細胞の予備処理、融合条件、融合細胞の選択採取方法、確認手段等を記載する。
- (ⅳ)
-
組換えタンパク質
組換えタンパク質の製造方法としては、組換えタンパク質をコードする遺伝子・発現に使用するベクター・宿主等の入手手段、該遺伝子の宿主への導入方法、該遺伝子を導入した形質転換体からの組換えタンパク質の採取・精製工程、組換えタンパク質の確認手段等を記載する。
(組換えタンパク質を包括的に記載した場合の実施可能要件の考え方については上記「(ⅰ)遺伝子、ベクター又は組換えベクター」の項参照。)
- (ⅴ)
-
モノクローナル抗体
モノクローナル抗体の製造方法としては、免疫原の入手・製造手段、免疫方法、抗体産生細胞の選択採取方法、モノクローナル抗体の確認手段等を記載する。
- (ⅵ)
-
微生物等の寄託(微生物等の寄託及び分譲の詳細については、「5.1微生物の寄託及び分譲」参照)
(a)微生物等(ここにおいて「微生物等」には微生物、植物、動物が含まれる。)から製造される遺伝子、ベクター、組換えベクター、形質転換体、融合細胞、組換えタンパク質、モノクローナル抗体等の発明においては、当該物を当業者が製造することができるよう、その製造方法を出願当初の明細書に記載するとともに、それらの製造のために使用する微生物等を当業者が容易に入手することができる場合(5.1(ⅱ)(b)参照)を除いて、その微生物等を寄託し、その受託番号を出願当初の明細書に記載する。
(b)遺伝子、ベクター、組換えベクター、形質転換体、融合細胞、組換えタンパク質、モノクローナル抗体等の発明において、当該物を当業者が製造できるように明細書に記載することができない場合には、製造された遺伝子・ベクター・組換えベクターが導入された形質転換体(組換えタンパク質を産生する形質転換体を含む)、融合細胞(モノクローナル抗体を産生するハイブリドーマを含む。)を寄託し、その受託番号を出願当初の明細書に記載する。
(c)限定的な条件を満たすモノクローナル抗体(例えば、限定的な結合定数により抗原Aに対する親和性を特定したモノクローナル抗体)を産生するハイブリドーマを取得することは、再現性がない場合が多いので、限定的な条件を満たすモノクローナル抗体に係る発明、及び該モノクローナル抗体を産生するハイブリドーマに係る発明においては、明細書の記載に基づいて当業者がその物を製造することができる場合を除き、該ハイブリドーマを寄託し、その受託番号を出願当初の明細書に記載することが必要である。
- ③
-
使用できること
遺伝子、ベクター、組換えベクター、形質転換体、融合細胞、組換えタンパク質、モノクローナル抗体等の発明においては、当業者がその物を使用できるように記載しなければならない。これは、発明の詳細な説明において示されていることが必要であるから、どのように使用できるかについて具体的な記載がなくても明細書及び図面の記載並びに出願時の技術常識に基づき当業者がその物を使用できる場合を除き、どのように使用できるかについて具体的に記載しなければならない。
例えば、遺伝子に係る発明が使用できることを示すためには、遺伝子が特定の機能(ここでいう「特定の機能」とは、「技術的に意味のある特定の用途が推認できる機能」のことである。)を有すること(例えば、構造遺伝子に係る発明の場合には、該遺伝子によりコードされるタンパク質が特定の機能を有すること)を発明の詳細な説明に記載する必要がある。
請求項において包括的に記載された遺伝子が、その機能により特定して記載されていない場合(単に「置換、欠失若しくは付加された」、「ハイブリダイズする」又は「○○%以上の相同性を有する」等の表現のみで記載された遺伝子)には、通常、当該包括的に記載された遺伝子に当該機能を有しないものが含まれるので、該遺伝子のうちの一部が使用できないことになり、当業者がその物を使用することができるように発明の詳細な説明が記載されていないことになる。
- (2)
-
方法の発明について
方法の発明について「実施をすることができる」とは、その方法を使用できることを意味する。また、発明の詳細な説明において、当該「方法の発明」について明確に説明されていることが必要である。この場合、当業者がその方法を使用できるように記載するために、必要に応じて 「(1)物の発明について」の実施可能要件を参照する。例えば、微生物等の寄託が必要な場合には、「5.1微生物等の寄託及び分譲」等を参照する。
- (3)
-
物を生産する方法の発明について
物を生産する方法の発明について「実施をすることができる」とは、その方法により物を作ることができることを意味する。また、発明の詳細な説明において、当該「物を生産する方法の発明」について明確に説明されていることが必要である。
したがって、遺伝子、ベクター、組換えベクター、形質転換体、融合細胞、組換えタンパク質、モノクローナル抗体等の製造方法の発明においては、当該方法について明確に説明するとともに、当業者がその方法により当該物を製造できるように記載することが必要である。この場合、当業者がその方法により当該物を製造できるように記載するために、必要に応じて「(1) 物の発明について」の実施可能要件を参照する。例えば、微生物等の寄託が必要な場合には、「5.1微生物等の寄託及び分譲」等を参照する。
また、その方法がどのように使用できるか又は当該物の少なくとも一つの用途を記載することが必要である。
- (4)
-
説明の具体化の程度について
発明の詳細な説明には、請求項に係る発明をどのように実施するかを示す「発明の実施の形態」のうち特許出願人が最良と思うものを少なくとも一つ記載することが必要であるが、「発明の実施の形態」の記載は、当業者が発明を実施できるように発明を説明するために必要である場合には、実施例を用いて行う。実施例とは、発明の実施の形態を具体的に示したもの(例えば物の発明の場合には、どのように作り、どのような構造を有し、どのように使用するか等を具体的に示したもの)である。
一般に物の構造や名称からその物をどのように作り、どのように使用するかを理解することが困難な技術分野に属する発明については、当業者がその発明の実施をすることができるように発明の詳細な説明を記載するためには、通常、一つ以上の代表的な実施例が必要である。
本技術分野は、物の構造からその物をどのように作り、どのように使用するかを理解することが困難な技術分野であるから、通常、一つ以上の実施例が必要である。
- (5)
-
請求項の記載と発明の詳細な説明との関係
発明の詳細な説明には、請求項に係る発明についてその実施の形態を少なくとも一つ記載することが必要であるが、請求項に係る発明に含まれるすべての下位概念又はすべての選択肢について実施の形態を示す必要はない。
しかし、当業者が、明細書及び図面の記載並びに出願時の技術常識に基づいて、発明の詳細な説明に記載された特定の実施の形態を、請求項に係る発明に含まれる他の部分についての実施にまで拡張することができないと信じるに足る十分な理由がある場合には、請求項に係る発明は当業者が実施できる程度に明確かつ十分に説明されていないものとする。この場合、審査官は、その理由を具体的に示すことが必要であり、その理由はできる限り文献を引用して示すことが好ましい。
 1.1.2.2 委任省令要件
1.1.2.2 委任省令要件
委任省令で求められる事項とは、(1)「発明の属する技術の分野」、及び(2)「発明が解決しようとする課題及びその解決手段」である。
- (1)
-
発明の属する技術の分野
発明の属する技術の分野として、原則として請求項に係る発明が属する技術の分野を少なくとも一つ記載する。
遺伝子工学に係る発明の場合、例えば、医薬品、分析試薬、植物育種のように記載する。
- (2)
-
発明が解決しようとする課題及びその解決手段
原則として、発明が解決しようとする課題としては、請求項に係る発明が解決しようとする技術上の課題を少なくとも一つ記載する。またその解決手段としては、請求項に係る発明によってどのように課題が解決されたかについて説明する。
例えば、A耐病性の遺伝子Bを導入したベクターを用いてA耐病性の植物を作出する方法の発明の場合、発明が解決しようとする課題としては「A耐病性の植物を作出すること」のように記載し、その解決手段としては、「A耐病性をもつ他の植物の染色体DNAから病原耐性遺伝子Bをクローニングし、該遺伝子を組み込んだ組換えベクターを得て、該組換えベクターにより形質転換した植物の細胞から植物体を再分化すること」のように記載する。
 1.1.2.3 従来技術及び有利な効果について
1.1.2.3 従来技術及び有利な効果について
- (1)
-
従来の技術
従来技術の記載から発明が解決しようとする課題が理解できる場合には、出願人が知る限りにおいて、請求項に係る発明の技術上の意義の理解及び特許性の審査に役立つと考えられる背景技術を記載すべきである。
また、従来の技術に関する文献は、請求項に係る発明の特許性を評価する際の重要な手段の一つであるから、特許を受けようとする発明と関連の深い文献が存在するときは、その文献名を記載すべきである。
- (2)
-
従来技術と比較した場合の有利な効果
請求項に係る発明が引用発明と比較して有利な効果がある場合には、請求項に係る発明の進歩性を肯定的に推認するのに役立つ事実として、これが参酌されるから、請求項に係る発明が有利な効果を有する場合には、出願人が知る限りにおいて、その有利な効果を記載すべきである。
 1.1.3 配列表
1.1.3 配列表
- (1)
-
10以上のヌクレオチドからなる核酸の塩基配列又は4以上のL-アミノ酸が結合したタンパク質若しくはペプチドのアミノ酸配列を明細書、特許請求の範囲又は図面中に記載する場合には、当該配列を含む配列表を、特許庁公報に公示する「塩基配列又はアミノ酸配列を含む明細書等の作成のためのガイドライン」(付録3)に示した作成方法に従ってコードデータにより作成し、明細書の最後にその一部分として記載する。(施行規則第24条様式29備考17参照。)
- (2)
-
塩基配列又はアミノ酸配列を特許請求の範囲に記載する場合には、「塩基配列又はアミノ酸配列を 含む明細書等の作成のためのガイドライン」に従って作成した配列表に記載された配列を引用することができる。
 1.2 発明の単一性
1.2 発明の単一性
次のような場合には、同一の又は対応する特別な技術的特徴があるので、一の願書で出願することができる。
なお、以下の事例では、各請求項に係る発明は、先行技術に対する貢献をもたらしているものとして説明する。
[例1]
請求項1 : タンパク質X
請求項2 : タンパク質Xをコードする構造遺伝子Y
請求項3 : 構造遺伝子Yを含む組換えベクターZ
請求項4 : 組換えベクターZを含む形質転換体A
(説明)
タンパク質Xは構造遺伝子Yによりコードされ、発現されるものであるから、両者は対応する特別な技術的特徴を有しているといえる。さらに、構造遺伝子Y、構造遺伝子Yを含む組換えベクターZ及び組換えベクターZを含む形質転換体Aは、すべて構造遺伝子Yという同一の特別な技術的特徴を有している。したがって、請求項1~4に係る発明は、同一の又は対応する特別な技術的特徴を有しているから、単一性の要件を満たす。
[例2]
請求項1 : 親細胞A
請求項2 : 親細胞Aを用いた融合細胞
(説明)
融合細胞は、親細胞Aと共通の特性を発揮するために不可欠な遺伝物質を、その遺伝物質の一部として包含するものであり、両者は同一の又は対応する特別な技術的特徴を有している。したがって、請求項1及び2に係る発明は、単一性の要件を満たす。
[例3]
請求項1 : 形質転換体A
請求項2 : 形質転換体Aによる化学物質Xの製造方法
(説明)
形質転換体Aによる化学物質Xの製造方法は、形質転換体Aに特有な性質・機能を使用しているものであるから、請求項2の製造方法は、請求項1の形質転換体Aを使用することに適している。したがって、これらは、同一の又は対応する特別な技術的特徴を有しているものであり、請求項1及び2に係る発明は、単一性の要件を満たす。
[例4]
請求項1 : 遺伝子Y
請求項2 : 遺伝子Yを用いる組換えベクターZの製造方法
請求項3 : 組換えベクターZを用いる形質転換体Aの製造方法
(説明)
請求項1~3の発明の特別な技術的特徴は、すべて遺伝子Yであり共通している。したがって、請求項1~3に係る発明は、単一性の要件を満たす。
[例5]
請求項1 : 抗原タンパク質X
請求項2 : 抗原タンパク質Xに対するモノクローナル抗体
(説明)
請求項2のモノクローナル抗体は、請求項1の抗原タンパク質Xを用いて初めて得られるものであり、また、請求項1記載の抗原タンパク質Xの検出、精製等に用いられるものであるから、両者は、その技術上の意義が密接に関係している。したがって、請求項1及び2に係る発明は、対応する特別な技術的特徴を有しており、単一性の要件を満たす。
次のような場合には、当該出願は、第37条 の要件を満たさない。
の要件を満たさない。
[例6]
請求項1 : 形質転換体A
請求項2 : 形質転換体Aにより生産された化学物質Xを使用する方法
- (注)
-
化学物質Xは公知である。
(説明)
形質転換体Aにより生産された化学物質Xの使用方法は、形質転換体Aに由来する特有な性質・機能を利用するものではなく、形質転換体Aを提供することと、化学物質Xを使用することは、技術上の意義が密接に関連していないので、同一の又は対応する特別な技術的特徴を有していない。したがって、請求項1及び2に係る発明は、単一性の要件を満たさない。
 1.3 特許要件
1.3 特許要件
 1.3.1 「産業上利用することができる発明」に該当しないもの
1.3.1 「産業上利用することができる発明」に該当しないもの
遺伝子、ベクター、組換えベクター、形質転換体、融合細胞、組換えタンパク質、モノクローナル抗体の発明において、それらの有用性が明細書、特許請求の範囲又は図面に記載されておらず、かつ何らそれらの有用性が類推できないものは、業として利用できない発明であり、第29条第1項柱書 の要件に違反する。
の要件に違反する。
 1.3.2 新規性
1.3.2 新規性
- (1)
-
組換えタンパク質
- ①
-
タンパク質が単離・精製された単一物質として公知である場合において、製造方法により特定して記載された組換えタンパク質に係る発明は、上記公知のタンパク質と物質として区別ができない場合、当該発明は新規性を有しない。
- ②
-
製造方法により特定して記載された組換えタンパク質に係る発明において、異なる宿主を用いたことにより、公知のタンパク質と糖鎖等に差異を有する組換えタンパク質が得られた場合には、該公知のタンパク質とアミノ酸配列においては区別できなくても、当該発明は新規性を有する。
- (2)
-
モノクローナル抗体
- ①
-
抗原Aが新規であれば、該抗原Aに対するモノクローナル抗体は、通常新規性を有する。
ただし、公知の抗原A’に対するモノクローナル抗体が公知であり、抗原Aが公知の抗原A’を一部改変したもの等であって該抗原A’と同一のエピトープを有しているものである場合、抗原A’に対するモノクローナル抗体は抗原Aにも反応する。よって、このような場合、「抗原Aに対するモノクローナル抗体」の発明は、新規性を有しない。
- ②
-
抗原Aに結合するモノクローナル抗体が公知である場合、抗原Aとは異なる抗原Bとの交差反応性を以て特定された「抗原Aに反応し、抗原Bに反応しないモノクローナル抗体」の発明は、該交差反応性でモノクローナル抗体を特定したことに特段の技術的意義がないとき(抗原Bが機能、構造等において特に抗原Aとの間に類似点がないために、公知の抗原Aに対するモノクローナル抗体も抗原Bとは反応しないことが明らかであるとき等)には新規性を有しない。
 1.3.3 進歩性
1.3.3 進歩性
- (1)
-
遺伝子
- ①
-
タンパク質Aが新規性及び進歩性を有する場合、タンパク質Aをコードする遺伝子に係る発明は、進歩性を有する。
- ②
-
タンパク質Aは公知であるが、そのアミノ酸配列は公知ではない場合、タンパク質Aをコードする遺伝子に係る発明は、タンパク質Aのアミノ酸配列を出願時に当業者が容易に決定することができた場合には進歩性を有しない。ただし、該遺伝子が、特定の塩基配列で記載されており、かつ、タンパク質Aをコードする他の塩基配列を有する遺伝子に比較して、当業者が予測できない有利な効果を奏する場合には、進歩性を有する。
- ③
-
タンパク質Aのアミノ酸配列が公知である場合、タンパク質Aをコードする遺伝子に係る発明は、進歩性を有しない。ただし、該遺伝子が、特定の塩基配列で記載されており、かつ、タンパク質Aをコードする他の塩基配列を有する遺伝子に比較して、当業者が予測できない有利な効果を奏する場合には、進歩性を有する。
- ④
-
ある構造遺伝子が公知である場合、公知の構造遺伝子と同種由来であって、かつ公知の構造遺伝子と同一の性質・機能を有する、天然に存在する変異体(対立遺伝子変異体等)の構造遺伝子に係る発明は、進歩性を有しない。ただし、本願発明の構造遺伝子が上記公知の構造遺伝子に比較して、当業者が予測できない有利な効果を奏する場合には、進歩性を有する。
- (2)
-
組換えベクター
ベクター及び導入される遺伝子がそれぞれ公知であれば、それらの組合せによって作出された組換えベクターに係る発明は、進歩性を有しない。ただし、ベクター及び導入される遺伝子が公知であっても、それらの特定の組合せによって作出された組換えベクターが当業者が予測できない有利な効果を奏する場合には、進歩性を有する。
- (3)
-
形質転換体
宿主及び導入される遺伝子がそれぞれ公知であれば、それらの組合せによって作出された形質転換体に係る発明は、進歩性を有しない。ただし、宿主及び導入される遺伝子が公知であっても、それらの特定の組合せによって作出された形質転換体が当業者が予測できない有利な効果を奏する場合には、進歩性を有する。
- (4)
-
融合細胞
親細胞がいずれも公知である場合、親細胞を融合して得られた融合細胞に係る発明は、進歩性を有しない。ただし、融合細胞が当業者が予測できない有利な効果を奏する場合には、融合細胞に係る発明は、進歩性を有する。
- (5)
-
モノクローナル抗体
抗原Aが公知であり、抗原Aが免疫原性を有することが明らかな場合(例えば抗原Aに対するポリクローナル抗体が公知であるか、抗原Aが分子量の大きいポリペプチドである等、免疫原性を有することが明らかである場合)には、「抗原Aに対するモノクローナル抗体」の発明は進歩性を有しない。ただし、他の特性等によりさらに特定された発明であって、その発明が当業者が予測できない有利な効果を奏する場合には、進歩性を有する。
 1.4 明細書、特許請求の範囲又は図面の補正
1.4 明細書、特許請求の範囲又は図面の補正
微生物等の寄託に関連した明細書、特許請求の範囲又は図面の補正については、「2.3 明細書、特許請求の範囲又は図面の補正」と同様に取り扱う。
 2. 微生物
2. 微生物
ここでは、微生物自体の発明、微生物の利用に関する発明などを取り扱う。微生物の利用に関する発明としては、新規な微生物の利用に限らず、公知微生物の利用方法を発見したことに基づく発明(例えば、公知微生物による物質の製造方法の発明、公知微生物による物の処理方法(例:水処理、土壌改善)の発明、公知微生物からなる処理剤(例:水処理剤、土壌改善剤)の発明)も含まれる。
微生物とは、酵母、カビ、キノコ、細菌、放線菌、単細胞藻類、ウイルス、原生動物などを意味し、さらには、動物又は植物の分化していない細胞及び組織培養物も含まれる。
また、微生物に関する発明であっても、遺伝子工学に関連する事項は「1. 遺伝子工学」を参照する。
 2.1 明細書及び特許請求の範囲の記載要件
2.1 明細書及び特許請求の範囲の記載要件
 2.1.1 微生物の表示
2.1.1 微生物の表示
微生物の表示は、原則として微生物の命名法による学名に従うものとする。
微生物の菌株を表示する場合には、原則として種名(微生物の命名法による)を付した菌株名で表示する。ただし、種名を特定することができない場合には、属名を付した菌株名で表示することができる。
微生物の菌株が寄託されている場合には、種名又はその種名を付した菌株名に加え、受託番号を記載することにより、当該菌株を表示することができる。
- 例:
-
バチルス ズブチルス (Bacillus subtilis) FERM P‐○○○○○菌株
また、動物又は植物の分化していない細胞は、原則として動物又は植物の命名法による学名又は標準和名に従うものとする。
 2.1.2 特許請求の範囲
2.1.2 特許請求の範囲
第36条第6項第2号 の規定は特許を受けようとする発明が明確であることを要件としていることから、特許請求の範囲は、一の請求項から発明が明確に把握されるように記載しなければならない。
の規定は特許を受けようとする発明が明確であることを要件としていることから、特許請求の範囲は、一の請求項から発明が明確に把握されるように記載しなければならない。
 2.1.3 発明の詳細な説明
2.1.3 発明の詳細な説明
(1.1.2参照)
 2.1.3.1 実施可能要件
2.1.3.1 実施可能要件
(1.1.2.1参照)
- (1)
-
物の発明について
物の発明において、創製される微生物や利用される微生物については以下のように記載する。
- ①
-
微生物について明確に説明されていること
微生物を明確に説明するためには、微生物の記載は以下のように行う。
新規な微生物を記載する場合には、微生物の命名法による種名、又はその種名を付した菌株名で表示し、菌学的性質を併せて記載する。菌学的性質としては、その分野で一般的に用いられている分類学的性質(付録1)を使用することが望ましいが、他の菌学的性質(例:代謝生産物の選択生産性)により記載することもできる。
なお、種名を特定することができない場合には、その理由を明確にした上で、属名を付した菌株名で表示する。
微生物の菌学的性質については、それが新菌株であるか、又は新種であるかにより、それぞれ以下のように記載する。
- (ⅰ)
-
新菌株である場合
菌株の特徴及び同種内の公知の菌株との相違点(菌学的性質)を明確に記載する。
- (ⅱ)
-
新種である場合
その分類学的性質を詳細に記載し、それを新種として判定した理由を明確にする。すなわち、在来の類似種との異同を明記し、その判定の根拠となった関連文献名を記載する。
- ②
-
作ることができること
微生物自体の発明又は新規微生物の利用に関する発明においては、当業者がその微生物を製造することができるようその創製手段を記載する。
創製手段とは、スクリーニング手段、突然変異作出手段、遺伝子組換え手段などをいう。
発明の詳細な説明に当業者がその微生物を製造することができるようにその創製手段を記載することができない場合には、特許法施行規則第27条の2の規定に従って、微生物を寄託する必要がある(詳細は「5.1微生物の寄託及び分譲」を参照)。
- ③
-
使用できること
微生物自体の発明又は微生物の利用に関する発明においては、当業者がその物を使用できるように記載しなければならない。これは、発明の詳細な説明において示されていることが必要であるから、どのように使用できるかについて具体的な記載がなくても明細書及び図面の記載並びに出願時の技術常識に基づき当業者がその物を使用できる場合を除き、どのように使用できるかについて具体的に記載しなければならない。
- (2)
-
方法の発明について
微生物の利用に関する発明のうち、微生物の使用方法の発明(例えば、微生物による物の処理方法の発明)については、以下のように記載する。
方法の発明について「実施をすることができる」とは、その方法を使用できることを意味する。また、発明の詳細な説明において、当該「方法の発明」について明確に説明されていることが必要である。
この場合、当業者がその方法を使用できるように記載するために、必要に応じて 「(1) 物の発明について」の実施可能要件を参照する。例えば、微生物の寄託が必要な場合には、「5.1微生物の寄託及び分譲」を参照する。
- (3)
-
物を生産する方法の発明について
微生物の利用に関する発明のうち、微生物を用いた物質の製造方法の発明については、以下のように記載する。
物を生産する方法の発明について「実施をすることができる」とは、その方法により物を作ることができることを意味する。また、発明の詳細な説明において、当該「物を生産する方法の発明」について明確に説明されていることが必要である。
したがって、微生物を用いた物質の製造方法の発明においては、当該方法について明確に説明するとともに、当業者がその方法により当該物を製造できるように記載することが必要である。この場合、当業者がその方法により当該物質を製造できるように記載するために、必要に応じて「(1)物の発明について」の実施可能要件を参照する。例えば、微生物の寄託が必要な場合には、「5.1微生物の寄託及び分譲」を参照する。
また、その方法がどのように使用できるか又は当該物質の少なくとも一つの用途を記載することが必要である。
なお、「説明の具体化の程度について」、「請求項の記載と発明の詳細な説明との関係」については、「1.遺伝子工学」の該当箇所 (1.1.2.1(4)及び(5)) を参照。
 2.1.3.2 委任省令要件
2.1.3.2 委任省令要件
委任省令で求められる事項とは、(1)「発明の属する技術の分野」、及び(2)「発明が解決しようとする課題及びその解決手段」である。
- (1)
発明の属する技術の分野
発明の属する技術の分野として、原則として請求項に係る発明が属する技術の分野を少なくとも一つ記載する。
微生物に係る発明の場合、例えば、医薬品、飼料、食品、水処理のように記載する。
- (2)
-
発明が解決しようとする課題及びその解決手段
原則として、発明が解決しようとする課題としては、請求項に係る発明が解決しようとする技術上の課題を少なくとも一つ記載する。またその解決手段としては、請求項に係る発明によってどのように課題が解決されたかについて説明する。
「従来技術及び有利な効果について」については、「1.遺伝子工学」1.1.2.3参照。
 2.2 特許要件
2.2 特許要件
 2.2.1 「産業上利用することができる発明」に該当しないもの
2.2.1 「産業上利用することができる発明」に該当しないもの
次の発明は、第29条第1項柱書 に規定する要件を満たしていない。
に規定する要件を満たしていない。
- (1)
-
単なる発見であって創作でないもの
- 例:
-
天然にある微生物を単に発見したもの
ただし、天然物から人為的に単離した微生物に係るものには創作性がある。
- (2)
-
その発明が業として利用できないもの
微生物自体の発明において、微生物の有用性が記載されておらず、かつ、何らその有用性が類推し得ないもの。
 2.2.2 進歩性
2.2.2 進歩性
- (1)
-
微生物自体の発明
微生物自体の発明の進歩性は、微生物の分類学的性質、及び微生物の利用上の効果に基づいて判断する。
- ①
-
その発明の微生物が、公知種と分類学的性質において著しい差異があるもの(新種)は、進歩性を有する。
- ②
-
その発明の微生物が、公知種と分類学的性質において著しい差異がない場合でも、その利用上、当業者が予測できない有利な効果を奏するものは、進歩性を有する。
- 例:
-
公知種に変異処理を施して得られた微生物で、その微生物の代謝生産物の生産性が顕著なもの
- (2)
-
微生物の利用に関する発明
- ①
-
微生物の利用に関する発明(例:物質を生産する方法の発明)において、利用する微生物が分類学上公知の種で、しかもその発明と同一の利用の態様(例:目的とする物質を生産すること)が知られている他の微生物と同一属に属する場合、通常その発明は進歩性を有しない。ただし、前者の微生物を利用したことが後者の微生物を利用したことに比較して、当業者が予測できない有利な効果を奏する場合には、その発明は進歩性を有する。
- (説明)
-
同一属内の公知菌種間であれば、それぞれの微生物を培養し、その利用性(例えば物質生産性)と効果を確認することは、通常容易に行いうるものである。
- ②
-
微生物の利用に関する発明(例:物質を生産する方法の発明)において、利用した微生物が公知種と分類学的性質において著しい差異があるもの(新種)である場合には、その利用の態様(例:目的とする物質)が同じであってもその発明は進歩性を有する。
- (説明)
-
上記(1)①に示したように、利用した微生物自体が進歩性を有するから、そのような微生物を利用する方法は進歩性を有する。
 2.3 明細書、特許請求の範囲又は図面の補正
2.3 明細書、特許請求の範囲又は図面の補正
- (1)
-
出願当初の明細書、特許請求の範囲又は図面に微生物が特定できるに足る菌学的性質が記載されており、かつ寄託機関名などの記載によりその微生物の寄託が特定できる場合には、受託番号を変更又は追加する補正は新たな技術的事項を導入するものではないから許される。
- (2)
-
利用した微生物が信用できる公的保存機関に保存されており、その保存番号が出願当初の明細書、特許請求の範囲又は図面に明示してあるものについて、微生物の同一性が失われないことが明らかな場合に限り、その後にその保存番号を特許手続上の寄託機関への寄託に基づく受託番号に変更する補正は新たな技術的事項を導入するものではないから許される。
この場合、受託番号の補正は、速やかに行う。
- (3)
-
出願当初の明細書、特許請求の範囲又は図面に、特許庁長官の指定する機関が発行する受領番号が記載されている場合、それと対応する受託番号に補正することは当然許される。(特許庁長官の指定する機関においては、受領番号は受託番号の先頭に「A」を付加したものに相当する。)
この場合、受託番号の補正は、速やかに行う。
- (4)
-
出願当初の明細書、特許請求の範囲又は図面に記載された受託番号を変更せず、かつ当初明細書、特許請求の範囲又は図面に当該微生物の分類学上の種が特定できる程度に菌学的性質が記載されている場合であっても、菌学的性質の追加補正は出願当初の明細書、特許請求の範囲又は図面の記載から自明な事項でない場合には、通常、新たな技術的事項を導入するものとなるから、その補正は許されない。(第Ⅲ部第Ⅰ節参照)
 3. 植物
3. 植物
ここでは、植物自体の発明、植物の部分(例:果実)に関する発明、植物の作出方法の発明、植物の利用に関する発明などを取り扱う。植物とは、生物を微生物、植物及び動物の三つに分類した場合の植物を意味する。
分化していない植物の細胞及び組織培養物は、微生物として取り扱うので、「2.微生物」の該当部分を参照する。
また、植物に関する発明であっても、遺伝子工学に関連する事項については, 「1.遺伝子工学」を参照する。
 3.1 明細書及び特許請求の範囲の記載要件
3.1 明細書及び特許請求の範囲の記載要件
 3.1.2 特許請求の範囲
3.1.2 特許請求の範囲
植物に係る発明においては、請求項は以下のように記載する。
植物自体の発明、植物の部分の発明、植物の利用に関する発明において、植物の特定は、例えば、植物の種類、当該植物が有する特徴となる遺伝子、当該植物が有する特性等の組合せによって行い、さらに作出方法を加えて特定してもよい。
- 例1:
-
樹皮中にカテコールタンニン含有量とピロガロールタンニン含有量がX1~X2:Y1~Y2の割合で含まれ、かつカテコールタンニンをZ1~Z2ppm(重量比)含む日本栗に属する植物であって受託番号がATCC‐○○○○○のもの又は上記特性を有する変異体。
- 例2:
-
2倍体のスイカを倍数化処理して得られる4倍体のスイカと2倍体のスイカを交配することにより得られる体細胞染色体数が33であるスイカ。
植物の作出方法の発明においては、請求項には、作出過程を順を追って記載する。作出過程の一つとして特性などによる選抜を行っている場合にはその選抜をする上で必要な特性等を、また環境等の条件が作出方法として必要な場合には、それらの条件を記載する。
- 例:
-
受託番号ATCC‐○○○○であるキャベツを種子親、他のキャベツを花粉親として、××除草剤に対する抵抗性を有するキャベツを得ることを特徴とする、キャベツの作出方法。
 3.1.3 発明の詳細な説明
3.1.3 発明の詳細な説明
(1.1.2参照)
 3.1.3.1 実施可能要件
3.1.3.1 実施可能要件
(1.1.2.1参照)
- (1)
-
物の発明について
植物自体の発明及び植物の部分の発明については以下のように記載する。
- ①
-
植物について明確に説明されていること
植物について明確に説明するために、例えば(ⅰ)作出された植物の種類に関する事項、(ⅱ)作出された植物の特徴となる特性に関する事項等を記載する。
- (ⅰ)
-
作出された植物の種類
原則として、植物命名法による学名又は標準和名を用いて記載する。
- (ⅱ)
-
作出された植物の特徴となる特性
作出された植物の特性に特徴がある場合には、それらについて実際に計測される数値等で具体的に記載し、必要に応じて公知の植物と比較して記載することが望ましい。
例えば、単に収量が多いという記載ではなく、1株当り総果数、1株当り総果重量或いは1アール当り総収量の如く、従来の収量調査で慣用されている方法で具体的数値を記載し、必要に応じて公知の植物と比較して記載する。
葉色、果色、花色等、色に関する記載については、色の三属性による表示法JIS Z8721の標準色票、色名に関するJIS Z8102又はR.H.S.カラーチャート等の公式の基準を用いて表現する。
なお、作出された植物の特徴となる特性が、当業者が通常行っている慣用栽培方法では発現されないとき、又は慣用栽培方法ではあるが特定の環境及び特定の栽培方法でしか発現しないような場合には、それらの特定の栽培条件を具体的に記載することが必要である。
- ②
-
作ることができること
植物自体の発明及び植物の部分の発明においては、親植物の種類、目的とする植物を客観的指標に基づいて選抜する方法等からなる作出過程を順を追って記載する。
発明の詳細な説明に当業者がその植物を製造することができるようにその創製手段を記載することができない場合には、特許法施行規則第27条の2の規定に従って、植物(その種子、細胞など)を寄託する必要がある。(植物の寄託及び分譲の詳細については、「5.2 植物の寄託及び分譲」参照。)
- ③
-
使用できること
植物自体の発明及び植物の部分の発明においては、当業者が使用できるように記載しなければならない。これは、発明の詳細な説明において示されていることが必要であるから、どのように使用できるかについて具体的な記載がなくても明細書及び図面の記載並びに出願時の技術常識に基づき当業者がその物を使用できる場合を除き、どのように使用できるかについて具体的に記載しなければならない。
- (2)
-
物を生産する方法の発明について
植物の作出方法の発明については、以下のように記載する。
植物の作出方法の発明においては、当業者がその方法により当該植物を作出できるように記載することが必要である。
この場合、当業者がその方法により当該植物を作出できるように記載するために、必要に応じて 「(1)物の発明について」の実施可能要件を参照する。例えば、植物の寄託が必要な場合には、「5.2 植物の寄託及び分譲」を参照する。
また、植物の作出方法の発明においては、明細書及び図面の記載並びに出願時の技術常識に基づき当業者がその方法又はその方法により作出された植物を使用できる場合を除き、発明の詳細な説明に、どのように使用ができるかについて記載しなければならない。
- (3)
-
方法の発明について
植物の利用に関する発明については、以下のように記載する。
方法の発明について「実施することができる」とは、その方法を使用できることを意味する。また、発明の詳細な説明において、当該「方法の発明」について明確に説明されていることが必要である。
この場合、当業者がその方法を使用できるように記載するために、必要に応じて「(1)物の発明について」の実施可能要件を参照する。例えば、植物の寄託が必要な場合には、「5.2 植物の寄託及び分譲」を参照する。
なお、「説明の具体化の程度について」、「請求項の記載と発明の詳細な説明との関係」、「委任省令要件」、「従来技術及び有利な効果について」については、「1. 遺伝子工学」の該当箇所 (1.1.2.1(4)及び(5)、1.1.2.2及び1.1.2.3)を参照。
 3.2 特許要件
3.2 特許要件
 3.2.1 「産業上利用することができる発明」に該当しないもの
3.2.1 「産業上利用することができる発明」に該当しないもの
次の発明は、 第29条第1項柱書 に規定する要件を満たしていない。
に規定する要件を満たしていない。
- (1)
-
単なる発見であって創作でないもの
- 例:
-
自然界で発見された植物そのもの
- (2)
-
その発明が業として利用できないもの
有用性が記載されておらず、かつ何ら有用性が類推できないもの。
 3.2.2 進歩性
3.2.2 進歩性
- (1)
-
植物自体の発明については、例えば、作出された植物の特性が、その植物が属する種の公知の植物の形質から容易に予測でき、かつ当業者が予測できない有利な効果を奏しない場合は、進歩性を有しない。
- 例1:
-
その植物が属する種の公知の植物と形状又は色彩が類似しているもの
- 例2:
-
その植物が属する種の植物の公知の形質の組み合わせにすぎないもの
(単なる交配によって得られたもの:例えば、さやが未熟のときには黄色い単一の遺伝子座により支配される形質を有する公知のエンドウAと全長にわたり節ごとに花がつく単一の遺伝子座により支配される形質を有する公知のエンドウBとを単に交配して形質を固定して得た、未熟のときに黄色く、節ごとに花がつく新規なエンドウは進歩性を有しない。)
- (2)
-
植物を作出する方法の発明については、例えば、親植物、手段、条件などの選択に困難性がなく、かつ作出された植物が当業者が予測できない有利な効果を奏しない場合は、進歩性を有しない。
 3.3 明細書、特許請求の範囲又は図面の補正
3.3 明細書、特許請求の範囲又は図面の補正
植物の寄託に関連した明細書、特許請求の範囲又は図面の補正については、「2.3 明細書、特許請求の範囲又は図面の補正」と同様に取り扱う。
 4. 動物
4. 動物
ここでは、動物自体の発明、動物の部分に関する発明、動物の作出方法の発明、動物の利用に関する発明などを取り扱う。動物とは、生物を、微生物、植物及び動物の三つに分類した場合の動物(人を除く。)を意味する。
分化していない動物の細胞及び組織培養物は、微生物として取り扱うので、「2. 微生物」の該当部分を参照する。
また、動物に関する発明であっても、遺伝子工学に関連する事項については、「1. 遺伝子工学」を参照する。
 4.1 明細書及び特許請求の範囲の記載要件
4.1 明細書及び特許請求の範囲の記載要件
 4.1.2 特許請求の範囲
4.1.2 特許請求の範囲
動物に係る発明においては、請求項は以下のように記載する。
動物自体の発明、動物の部分の発明、動物の利用に関する発明において、動物の特定は、例えば、動物の種類、当該動物が有する特徴となる遺伝子、当該動物が有する特性等の組合せによって行い、さらに作出方法を加えて特定してもよい。
- 例:
-
8週齢で水晶体前方皮質繊維の腫大変性がはじまり、5ないし6ヶ月齢で水晶体白濁が現れ始め、その直後速やかに白内障が完成するという特性を有するマウスであって、受託番号がDSM‐○○○○○のもの又は上記特性を有する変異体。
 4.1.3 発明の詳細な説明
4.1.3 発明の詳細な説明
(1.1.2参照)
 4.1.3.1 実施可能要件
4.1.3.1 実施可能要件
(1.1.2.1参照)
- (1)
-
物の発明について
動物自体の発明及び動物の部分の発明については以下のように記載する。
- ①
-
動物について明確に説明されていること
動物について明確に説明するために、例えば(ⅰ)作出された動物の種類に関する事項、(ⅱ)作出された動物の特徴となる特性に関する事項等を記載する。
- (ⅰ)
-
作出された動物の種類
原則として、動物命名法による学名又は標準和名を用いて記載する。
- (ⅱ)
-
作出された動物の特徴となる特性
作出された動物の特性に特徴がある場合には、それらについて実際に計測される数値等で具体的に記載し、必要に応じて公知の動物と比較して記載することが望ましい。
なお、作出された動物の特徴となる特性が、当業者が通常行っている慣用飼育条件では発現されず、特定の環境或いは特定の飼育条件でしか発現しないような場合には、それらの特定の飼育条件等を具体的に記載することが必要である。
- ②
-
作ることができること
動物自体の発明及び動物の部分の発明においては、親動物の種類、目的とする動物を客観的指標に基づいて選抜する方法等からなる作出過程を順を追って記載する。
発明の詳細な説明に当業者がその動物を製造することができるようにその創製手段を記載することができない場合には、特許法施行規則第27条の2の規定に従って、動物(その受精卵など)を寄託する必要がある。(動物の寄託及び分譲の詳細については、「5.3動物の寄託及び分譲」参照。)
- ③
-
使用できること
動物自体の発明においては、当業者がその物を使用できるように記載しなければならない。これは、発明の詳細な説明に記載されていることが必要であるから、どのように使用できるかについて具体的な記載がなくても明細書及び図面の記載並びに出願時の技術常識に基づき当業者がその物を使用できる場合を除き、どのように使用できるかについて具体的に記載しなければならない。
- (2)
-
物を生産する方法の発明について
動物の作出方法の発明については、以下のように記載する。
動物の作出方法の発明においては、当業者がその方法により当該動物を作出できるように記載することが必要である。
この場合、当業者がその方法により当該動物を作出できるように記載するために、必要に応じて「(1)物の発明について」の実施可能要件を参照する。例えば、動物の寄託が必要な場合には、「5.3動物の寄託及び分譲」を参照する。
また、動物の作出方法の発明においては、明細書及び図面の記載並びに出願時の技術常識に基づき当業者がその方法又はその方法により作出された動物を使用できる場合を除き、発明の詳細な説明に、どのように使用できるかについて記載しなければならない。
- (3)
-
方法の発明について
動物の利用に関する発明については、以下のように記載する。
方法の発明について「実施することができる」とは、その方法を使用できることを意味する。また、発明の詳細な説明において、当該「方法の発明」について明確に説明されていることが必要である。
この場合、当業者がその方法を使用できるように記載するために、必要に応じて「(1) 物の発明について」の実施可能要件を参照する。例えば、動物の寄託が必要な場合には、「5.3動物の寄託及び分譲」を参照する。
なお、「説明の具体化の程度について」、「請求項の記載と発明の詳細な説明との関係」、「委任省令要件」、「従来技術及び有利な効果について」については、「1. 遺伝子工学」の該当箇所 (1.1.2.1(4)及び(5)、 1.1.2.2及び1.1.2.3) を参照。
 4.2 特許要件
4.2 特許要件
 4.2.1 「産業上利用することができる発明」に該当しないもの
4.2.1 「産業上利用することができる発明」に該当しないもの
次の発明は、第29条第1項柱書 に規定する要件を満たしていない。
に規定する要件を満たしていない。
- (1)
-
単なる発見であって創作でないもの
- 例:
-
自然界で発見された動物そのもの
- (2)
-
その発明が業として利用できないもの
有用性が記載されておらず、かつ、何らその有用性が類推し得ないもの。
 4.2.2 公の秩序、善良の風俗又は公衆の衛生を害するおそれがある発明
4.2.2 公の秩序、善良の風俗又は公衆の衛生を害するおそれがある発明
実施が必然的に公序良俗又は公衆の衛生を害するおそれがある場合は、第32条 に該当する発明とな る。
に該当する発明とな る。
 4.3 明細書、特許請求の範囲又は図面の補正
4.3 明細書、特許請求の範囲又は図面の補正
動物の寄託に関連した明細書、特許請求の範囲又は図面の補正については、「2.3 明細書、特許請求の範囲又は図面の補正」と同様に取り扱う。
 5. 寄託
5. 寄託
ここでは、微生物、植物、動物など寄託を必要とする発明について取り扱う。
 5.1 微生物の寄託及び分譲
5.1 微生物の寄託及び分譲
微生物自体の発明又は新規微生物の利用に関する発明において、発明の詳細な説明に当業者がその微生物を製造することができるようにその創製手段を記載することができない場合には、特許法施行規則第27条の2の規定に従って、微生物を寄託する必要がある(詳細は以下を参照。(参考)微生物寄託範囲の拡大に伴う運用の変更についても参照。)。
特許法施行規則第27条の2(微生物の寄託)
- 微生物に係る発明について特許出願をしようとする者は、その発明の属する技術の分野における通常の知識を有する者がその微生物を容易に入手することができる場合を除き、その微生物の寄託について特許手続上の微生物の寄託の国際的承認に関するブダペスト条約(以下この条において「条約」という。)
- 第二条(ⅷ)の国際寄託当局の交付する条約に基づく規則第七規則の受託証のうち最新のものの写し又は特許庁長官の指定する機関にその微生物を寄託したことを証明する書面を願書に添付しなければならない。
- 2 特許出願の後に前項の微生物の寄託について新たな受託番号が付されたときは、特許出願人又は特許権者は、遅滞なく、その旨を特許庁長官に届け出なければならない。
- 3 前項の届出は、特許出願についてする場合は様式第三十三によりしなければならない。
特許法施行規則第27条の3(微生物の試料の分譲)
- 前条の規定により寄託された微生物に係る発明を試験又は研究のために実施しようとする者は、次に掲げる場合は、その微生物の試料の分譲を受けることができる。
- 一 その微生物に係る発明についての特許権の設定の登録があったとき。
- 二 特許法第六十五条第一項
 の規定によりその微生物に係る発明の内容を記載した書面を提示され警告を受けたとき。
の規定によりその微生物に係る発明の内容を記載した書面を提示され警告を受けたとき。 - 三 特許法第五十条
 (同法第百五十九条第二項
(同法第百五十九条第二項 (同法第百七十四条第一項
(同法第百七十四条第一項 において準用する場合を含む。)及び同法第百六十三条第二項
において準用する場合を含む。)及び同法第百六十三条第二項 において準用する場合を含む。)の意見書を作成するために必要なとき。
において準用する場合を含む。)の意見書を作成するために必要なとき。 - 2 前項の規定により微生物の試料の分譲を受けた者は、その微生物の試料を第三者に利用させてはならない。
- (ⅰ)
寄託及び分譲
微生物に係る発明について特許出願をしようとする者(以下、「出願人」という。)は、当業者がその微生物を容易に入手することができる場合を除き、その微生物を特許庁長官の指定する機関又は国際寄託当局(以下、両者を「特許手続上の寄託機関」という。)に寄託し、かつその受託番号を出願当初の明細書に明示するとともに、その事実を証明する書面(以下、「受託証の写し」という。)を当該出願の願書に添付しなければならない。
特許庁長官の指定する機関では、寄託申請を受け付けた際、直ちに「受領書」を発行し、生存確認試験を行って、微生物の生存を確認した後に「受託証」を交付する。「受領書」は、「受託証」と異なり、特許法施行規則第27条の2に規定される「特許庁長官の指定する機関にその微生物を寄託したことを証明する書面」ではないので、その写しを願書に添付する必要はない。
微生物の生存確認試験はある程度の時間を要するので、出願人は「受領書」に記載された受領番号を出願当初明細書に明示して特許出願をすることができる。この場合、出願人は、「受託証」が交付されたとき、速やかに特許庁へその写しを提出しなければならない。
「受託証」が交付されて初めて、当該微生物は当該受領日において寄託されたものとなるので、生存確認試験において生存が確認されず、「受託証」が交付されなかったときは、当該出願は受領日における寄託はなかったものとして取り扱われる。
また、特許出願の後に、再寄託、他の国際寄託当局への移送、又は国内寄託からブダペスト条約に基づく寄託への変更などにより、先の寄託微生物に新たな受託番号が付されたときは、特許出願人又は特許権者は遅滞なく、その旨を特許庁長官に届け出なければならない。特許庁長官の指定する機関に寄託され、該機関によって生存が確認された微生物が、その後生存しないことが明らかになった場合には、寄託者は、該機関から「分譲できない旨の通知」を受け取った後、速やかにもとの寄託に係る微生物と同一の微生物を寄託しなければならない。そして、当該微生物に係る発明についての特許出願人又は特許権者は、遅滞なく、その旨を特許庁長官に届け出なければならない。その場合、後の寄託はもとの寄託から引き続いて寄託されていたものとして取り扱う。
上記の寄託微生物は特許権の設定登録と同時に分譲可能な状態とされる。ただし、特許権の設定登録前であっても特許法施行規則第27条の3第1項第2号又は第3号に該当する場合には、その限りにおいて当該微生物は分譲可能な状態とされる。
寄託した微生物は少なくともその微生物に係る発明の特許権が存続する期間は、その微生物の分譲が可能な状態にあるように、その寄託が維持されなければならない。
なお、国際寄託当局及び各国際寄託当局が受理している寄託対象物の一覧表を付録2に示す。
- (ⅱ)
寄託義務から除外される微生物
- (a)
-
特許庁長官の指定する寄託機関において技術的理由等によって寄託ができない微生物
ただし、この場合において、特許法施行規則第27条の3に掲げた微生物の分譲については出願人が保証するものとする。(信用できる保存機関への保存等の手段を採ることが望ましい。)
- (b)
「特許法施行規則第27条の2」でいう当業者が容易に入手することができる微生物
具体的には、例えば以下のものをいう。
- (イ)
パン酵母、麹菌、納豆菌などの市販されている微生物
- (ロ)
-
信用できる保存機関に保存され、かつ保存機関の発行するカタログ等により自由に分譲されうることが出願前に明らかな微生物
この場合、当該微生物の保存番号を出願当初の明細書に記載するものとする。
- (ハ)
明細書の記載に基づいて当業者が製造しうる微生物
- (ⅲ)
優先権主張を伴う出願
優先権主張を伴う出願であって、その出願に係る発明が、当業者が容易に入手することができない微生物に係るものである場合には、その微生物が特許手続上の寄託機関又は信用できる公的保存機関に出願前に保管されており、その受託番号又は保存番号が優先権主張の基礎となる第一国の出願明細書中、又は国内優先権主張を伴う出願においては先の出願明細書中に記載されているときは、その出願について、優先権の効果を享受することができる。
- (ⅳ)
受託証の写しの提出の省略
同時に二以上の手続をする際に同一の受託証の写しを提出する場合あるいは他の出願で既に提出している受託証の写しと同じ受託証の写しを提出する場合は、特許法施行規則第10条第1項及び第2項の規定に従ってその旨を申し出て、受託証の写しの提出を省略することができる。
例えば、以下のような場合には、受託証の写しの提出を省略することができる。
- (1)
分割出願をする場合
- (2)
国内優先権の主張を伴う出願をする場合
- (3)
先にした出願と同一の受託証の写しを提出する必要がある同一出願人による出願をする場合
- (4)
同時に二以上の出願をし、同一の受託証の写しを提出する必要がある出願をする場合
- (5)
受託番号変更届を提出する場合
特許法施行規則第10条(提出書面の省略)
- 同時に二以上の手続(・・・)をする場合において、・・・第二十七条の二第一項若しくは第二項・・・の規定により提出すべき証明書の内容が同一であるときは、一の手続についてこれを提出し、他の手続においてその旨を申し出て当該証明書の提出を省略することができる。
- 2他の事件(・・・)について既に特許庁に証明書を提出した者は、・・・第二十七条の二第一項若しくは第二項・・・に規定する場合において、その事項に変更がないときは、当該手続においてその旨を申し出て当該証明書の提出を省略することができる。ただし、特許庁長官は、特に必要があると認めるときは、当該証明書の提出を命ずることができる。
 5.2 植物の寄託及び分譲
5.2 植物の寄託及び分譲
植物自体の発明、植物の部分に関する発明、植物の作出方法の発明、植物の利用に関する発明において、発明の詳細な説明に当業者がその植物を製造することができるようにその創製手段を記載することができない場合には、特許法施行規則第27条の2の規定に従って、植物を寄託する必要がある(詳細は「5.1微生物の寄託及び分譲」を参照)。
- (a)
-
明細書に作出過程を順を追って記載しても、親植物が容易に入手できないために当業者が実施をすることができない場合には、特許法施行規則第27条の2の規定に従って、親植物(その種子、細胞等)を出願前に寄託し、その受託番号を出願当初の明細書に記載する。
- (b)
-
当該植物を当業者が作出できるように明細書に記載することができない場合には、特許法施行規則第27条の2の規定に従って、複製可能な作出された植物(その種子、細胞等)を出願前に寄託し、その受託番号を出願当初の明細書に記載する。
ただし、特許庁長官の指定する寄託機関の技術的理由等によりそれらが寄託できない場合は、その入手手段を明細書に記載し、特許法施行規則第27条の3の規定に準じて、分譲は出願人が保証するものとする。(信用できる保存機関への保存等の手段を採ることが望ましい。)
 5.3 動物の寄託及び分譲
5.3 動物の寄託及び分譲
動物自体の発明、動物の部分に関する発明、動物の作出方法の発明、動物の利用に関する発明において、発明の詳細な説明に当業者がその動物を製造することができるようにその創製手段を記載することができない場合には、特許法施行規則第27条の2の規定に従って、動物を寄託する必要がある(詳細は「5.1微生物の寄託及び分譲」を参照)。
- (a)
-
明細書に作出過程を順を追って記載しても、親動物が容易に入手できないために当業者が実施をすることができない場合には、特許法施行規則第27条の2の規定に従って、親動物(その受精卵等)を出願前に寄託し、その受託番号を出願当初の明細書に記載する。
- (b)
-
当該動物を当業者が作出できるように明細書に記載することができない場合には、特許法施行規則第27条の2の規定に従って、複製可能な作出された動物(その受精卵等)を出願前に寄託し、その受託番号を出願当初の明細書に記載する。
ただし、特許庁長官の指定する寄託機関の技術的理由等によりそれらが寄託できない場合は、その入手手段を明細書に記載し、特許法施行規則第27条の3の規定に従って、分譲は出願人が保証するものとする。(信用できる保存機関への保存等の手段を採ることが望ましい。)
 6. 遺伝子関連発明事例集
6. 遺伝子関連発明事例集
[注]
以下の事例においては、特許法第29条第1項柱書き の要件については言及していない。各ケースにおいて、「相同性」の算出方法は明細書中に記載されており、該算出方法は技術的に妥当なものである。
の要件については言及していない。各ケースにおいて、「相同性」の算出方法は明細書中に記載されており、該算出方法は技術的に妥当なものである。
 6.1 単一性について
6.1 単一性について
発明の単一性の事例については、「第I部 第2章 発明の単一性の要件 5.事例集」のバイオテクノロジー発明の単一性に関する事例参照。
 6.2 実施可能要件が満たされない場合
6.2 実施可能要件が満たされない場合
事例1 全長cDNA
特許請求の範囲
【請求項1】
配列番号5で表されるDNA配列からなるポリヌクレオチド
発明の詳細な説明の概要
配列番号5で表されるDNA配列からなるポリヌクレオチドは、ヒト肝細胞cDNAライブラリーから取得された、3000個の塩基からなるcDNAである。また、該ポリヌクレオチドは、配列番号6で表される1000個のアミノ酸配列からなるポリペプチドをコードするものである。
そして、本願出願前に公開されていたDNA及びアミノ酸配列データベースを用いて、配列番号5及び6で表されるDNA及びアミノ酸配列のホモロジー検索を行ったところ、相同性が30%以上の配列は見出されなかった。一方、配列番号6で表されるアミノ酸配列の解析から、該ポリペプチドにはグリコシル化可能部位があることが判明した。
したがって、請求項1に係る発明のポリヌクレオチドは、未知の機能を持った、これまで知られていない糖タンパク質をコードするものである可能性があり、新たな医薬等の開発に有用なものである。
先行技術調査の結果
相同性が30%以上のDNA及びアミノ酸配列は発見されなかった。
拒絶理由の概要
糖タンパク質には様々な種類の機能を有するものが存在するので、該ポリヌクレオチドが例え糖タンパク質をコードするものであったとしても、該糖タンパク質がいかなる特定の機能を有するものであるかは不明である。
また、本願出願時の技術常識を考慮しても、「配列番号5で表されるDNA配列からなるポリヌクレオチド」が実際にどの様な特定の機能を有するタンパク質をコードするものであるかを予測することはできない。
そして、該ポリヌクレオチドがいかなる特定の機能を有するものかが不明である以上、どの様に使用できるのかも不明である。
したがって、請求項1に係る発明を当業者が実施をすることができる程度に明確かつ十分に、発明の詳細な説明が記載されているものとは認められない。
拒絶理由に対する対処
通常、上記の拒絶理由を解消することはできない。
(補足説明)
ここでいう「特定の機能」とは「技術的に意味のある特定の用途が推認できる機能」のことをいう。
事例2 全長cDNA
特許請求の範囲
【請求項1】
配列番号7で表されるDNA配列からなるポリヌクレオチド
発明の詳細な説明の概要
配列番号7で表されるDNA配列からなるポリヌクレオチドは、ヒト肝細胞cDNAライブラリーから取得された、2400個の塩基からなるcDNAである。また、該ポリヌクレオチドは、配列番号8で表される800個のアミノ酸配列からなるポリペプチドをコードするものである。
そして、本願出願前に公開されていたDNA及びアミノ酸配列データベースを用いて、配列番号7及び8で表されるDNA及びアミノ酸配列のホモロジー検索を行ったところ、それぞれ、文献A、B等に記載されたラット等いくつかの哺乳類のWW1因子をコードするDNA配列及び該WW1因子のアミノ酸配列と、20~30%の相同性を有していた。
したがって、請求項1に係る発明のポリヌクレオチドは、ヒトのWW1因子をコードするものであり、有用なものである。
先行技術調査の結果
相同性が40%以上のDNA及びアミノ酸配列は発見されなかった。
拒絶理由の概要
ヒトのWW1因子をコードするものであることの根拠としては、ラット等いくつかの哺乳類のWW1因子をコードするDNA配列及び該WW1因子のアミノ酸配列と20~30%の相同性を有していたことのみである。
ここで、一般に2つのポリヌクレオチド(ポリペプチド)間でのDNA(アミノ酸)配列の相同性が20~30%程度である場合、該2つのポリヌクレオチド(ポリペプチド)は互いに異なる特定の機能を有する蓋然性が高いといえる。また、あるポリヌクレオチド(ポリペプチド)が、WW1因子をコードするポリヌクレオチド(WW1因子)と相同性が20~30%程度あれば、該ポリヌクレオチドはWW1因子をコードする蓋然性が高いとの技術常識が本願出願時にあったともいえない。
よって、請求項1に係る発明のポリヌクレオチドは、実際にはWW1因子をコードしていない蓋然性が高いので、該ポリヌクレオチドがいかなる特定の機能を有するものかが不明であり、また、実際にどの様な特定の機能を有するタンパク質をコードするものであるかを予測することはできないので、どの様に使用できるのかも不明である。
したがって、請求項1に係る発明を当業者が実施をすることができる程度に明確かつ十分に、発明の詳細な説明が記載されているものとは認められない。
拒絶理由に対する対処
請求項1に係る発明のポリヌクレオチドが「ヒトのWW1因子」をコードすることを、実際に発現させたタンパク質の活性の提示、理論的な説明により意見書等で立証した場合、上記の拒絶理由は解消する場合がある。
(補足説明)
上記の理論的な説明が、本願出願前に公知の保存領域に関する知見に基づく場合は、該保存領域のDNA配列に基づいて調製したDNAプライマーを用いたPCR法等により、「WW1因子」をコードするポリヌクレオチドを当業者が容易に取得でき、かつ、該ポリヌクレオチドが予測しえない有利な効果を奏さないと判断された場合には、請求項1に係る発明の進歩性が欠如する旨の拒絶理由が存在することになる。
なお、ここでいう「特定の機能」とは「技術的に意味のある特定の用途が推認できる機能」のことをいう。
WW1因子の「特定の機能」、すなわち「技術的に意味のある特定の用途が推認できる機能」は知られている。
事例3 全長cDNA
特許請求の範囲
【請求項1】
配列番号9で表されるDNA配列からなるポリヌクレオチド
発明の詳細な説明の概要
配列番号9で表されるDNA配列からなるポリヌクレオチドは、ヒト肝細胞cDNAライブラリーから取得された、2400個の塩基からなるcDNAである。また、該ポリヌクレオチドは、配列番号10で表される800個のアミノ酸配列からなるポリペプチドをコードするものである。
そして、本願出願前に公開されていたDNA及びアミノ酸配列データベースを用いて、配列番号9及び10で表されるDNA及びアミノ酸配列のホモロジー検索を行ったところ、文献Aに記載されたラットのZZ1因子、文献Bに記載されたブタのZZ2因子、及び、文献Cに記載されたサルのZZ1因子受容体アンタゴニスト、それぞれのDNA及びアミノ酸配列と、20~30%の相同性を有していた。
したがって、請求項1に係る発明のポリヌクレオチドは、ヒトのZZ因子に関連したタンパク質をコードするものであり、ZZ因子に関連した疾病の治療等に有用なものである可能性がある。
先行技術調査の結果
相同性が40%以上のDNA及びアミノ酸配列は発見されなかった。
拒絶理由の概要
ヒトのZZ因子に関連したタンパク質には、互いに機能が異なるタンパク質であるZZ1因子、ZZ2因子、ZZ1因子受容体アンタゴニスト等が含まれるので、請求項1に係る発明のポリヌクレオチドが、例え、ヒトのZZ因子に関連したタンパク質をコードしているとしても、該タンパク質が実際にどの様な特定の機能を有するものであるかは依然として不明である。
また、本願出願時の技術常識を考慮しても、該ポリヌクレオチドが実際にどの様な特定の機能を有するタンパク質をコードするものであるかを予測することはできない。
そして、該ポリヌクレオチドがいかなる特定の機能を有するものかが不明である以上、どの様に使用できるのかも不明である。
したがって、請求項1に係る発明を当業者が実施をすることができる程度に明確かつ十分に、発明の詳細な説明が記載されているものとは認められない。
拒絶理由に対する対処
例えば、請求項1に係る発明のポリヌクレオチドが、ZZ因子関連タンパク質のうち「ヒトのZZ1因子」をコードすることを、意見書等で立証したとしても、通常、上記の拒絶理由は解消しない。
(補足説明)
本願明細書の「ラットのZZ1因子、ブタのZZ2因子、サルのZZ1因子受容体アンタゴニスト、それぞれのDNA及びアミノ酸配列と、20~30%の相同性を有していた」との記載及び「ヒトのZZ因子に関連したタンパク質をコードする」との記載からは、直ちに「ヒトZZ1因子をコードする」ことまでもが示されていたとは、本願出願時の技術常識から推認することはできない。
なお、ここでいう「特定の機能」とは「技術的に意味のある特定の用途が推認できる機能」のことをいう。
ZZ因子に関連するタンパク質であるZZ1因子、ZZ2因子、及び、ZZ1因子受容体アンタゴニストは、各々全く異なる「特定の機能」、すなわち「技術的に意味のある特定の用途が推認できる機能」を有するものであることが知られている。
 6.3 進歩性がない場合
6.3 進歩性がない場合
事例4 全長cDNA
特許請求の範囲
【請求項1】
配列番号11で表されるDNA配列からなるポリヌクレオチド
発明の詳細な説明の概要
配列番号11で表されるDNA配列からなるポリヌクレオチドは、ヒト肝細胞cDNAライブラリーから取得された、2700個の塩基からなるcDNAである。また、該ポリヌクレオチドは、配列番号12で表される900個のアミノ酸配列からなるポリペプチドをコードするものである。
そして、本願出願前に公開されていたDNA及びアミノ酸配列データベースを用いて、配列番号11及び12で表されるDNA及びアミノ酸配列のホモロジー検索を行ったところ、それぞれ、文献Aに記載されたラットのXX1因子をコードするDNA配列及び該XX1因子のアミノ酸配列と、80%及び85%の相同性を有していた。
したがって、請求項1に係る発明のポリヌクレオチドは、ヒトのXX1因子をコードするものであり、有用なものである。
先行技術調査の結果
上記以外に相同性が80%以上のDNA及びアミノ酸配列は発見されなかった。
ヒト等の哺乳動物がXX1因子を有することは、周知技術である。
拒絶理由の概要
あるタンパク質をコードするポリヌクレオチドを取得することは、本願出願前、周知の課題である。
そして、ある哺乳類のタンパク質をコードするポリヌクレオチドと、他の哺乳類の該タンパク質に対応するタンパク質をコードするポリヌクレオチドとは、一般に相同性が高いとの技術常識に基づき、ある哺乳類の既知のタンパク質をコードするポリヌクレオチドの一部をPCRプライマーとして用いて、他の哺乳類の該タンパク質に対応するタンパク質をコードするポリヌクレオチドをDNAプライマーを用いたPCR法等により取得することは、本願出願前、周知の技術である。
してみると、文献Aに記載されたラットのXX1因子をコードするポリヌクレオチドのDNA配列に基づいて作成したDNAプローブを用い、ヒトXX1因子を得るためにヒト由来のcDNAライブラリーからヒトのXX1因子をコードするポリヌクレオチドを取得することは、当業者が容易になし得ることである。そして、請求項1に係る発明のポリヌクレオチドが上記文献A及び周知技術から予測できない有利な効果を奏するものとも認められない。
拒絶理由に対する対処
本願出願時の技術水準では請求項1に係る発明のポリヌクレオチドを取得することが困難であった等の特段の事情がある場合は、その旨を意見書等で立証することにより、上記の拒絶理由は解消する場合がある。
(補足説明)
XX1因子の特定の機能、すなわち技術的に意味のある特定の用途が推認できる機能は知られている。
 6.4 進歩性がなく、かつ、実施可能要件が満たされない場合
6.4 進歩性がなく、かつ、実施可能要件が満たされない場合
事例5 DNA断片
特許請求の範囲
【請求項1】
配列番号13で表されるDNA配列からなるポリヌクレオチド
発明の詳細な説明の概要
cDNAライブラリーはオリゴdTプライマーを用いてヒトの肝臓から構築された。配列番号13で表されるDNA配列は、自動DNA配列決定装置を用いて分析された長さ500塩基の配列の1つである。
配列番号13の塩基配列からなるポリヌクレオチドは、構造遺伝子の一部であり、全長DNAを得るための段階の1つにおいて、プローブとして用いることができる。
しかしながら、全長DNAが実際に得られたことを示す実施例はなく、ポリヌクレオチドとそれが対応する蛋白質の機能や生理活性に関する記載もない。
先行技術調査の結果
相同性が30%以上のDNA及びアミノ酸配列は発見されなかった。
拒絶の理由の概要
1.進歩性について
ヒトの細胞からcDNAを取得し、配列を決定することは、周知の課題である。
また、肝臓等のヒト組織由来のcDNAライブラリーを構築し、そのライブラリーからランダムに選ばれたcDNAの配列を、自動配列決定装置を用いて分析することもまた、周知技術である。
してみると、周知技術を用いてcDNAライブラリーを構築し、そのライブラリーからランダムに選ばれたcDNAの配列を、自動配列決定装置を用いて分析して配列情報を取得することは、当業者が容易になし得ることである。そして、請求項1に係る発明のポリヌクレオチドが上記周知技術から予測できない有利な効果を有するものとも認められない。
2.実施可能要件について
物の発明についての実施できるとは、その物をつくることができ、かつ、その物を使用できることである。
発明の詳細な説明には、請求項1に係る発明のポリヌクレオチドは全長DNAを取得する段階の一つにおいてプローブとして使用できると記載されているが、対応する全長DNAにコードされるタンパク質の機能や生理活性に関する記載はなく、それらを予測することもできない。
対応するタンパク質の機能や生理活性が未知の全長DNAを取得するためにDNA断片を使用することは、上記「使用できること」に該当するとは認められない。したがって、請求項1に係る発明を当業者が実施できる程度に明確かつ十分に発明の詳細な説明が記載されているとは認められない。
拒絶理由に対する対処
通常、上記拒絶理由2を解消することはできない。
事例6 SNP
特許請求の範囲
【請求項1】
配列番号14又は15で表されるDNA配列からなるポリヌクレオチドにおいて、100番目の塩基(多型部位)を含む20~100の連続したDNA配列からなるポリヌクレオチド
発明の詳細な説明の概要
10人のゲノムDNA○○ローカス中500塩基分の配列を決定及び比較したところ、配列番号14で表されるDNAを有するヒトが6人、配列番号15で表されるDNAを有するヒトが4人であった。両配列は、100番目の塩基が配列番号14で表されるDNA配列ではgであるのに対して、配列番号15で表されるDNA配列ではcである点でのみ異なっている。
請求項1に係る発明のポリヌクレオチドは、法医学的鑑定に使用できる。
先行技術調査の結果
配列番号14及び15で表されるゲノムDNAの塩基配列は知られていない。さらに、請求項1に係る発明のポリヌクレオチドも知られていない。
拒絶理由の概要
1.進歩性について
ヒトゲノムDNAの多型部位を検出することは、当該分野における周知の課題である。
また、複数のヒト由来ゲノムDNAの塩基配列を決定し、その配列を比較することで多型部位を検出することは、当該分野における周知技術である。
してみると、複数のヒト由来ゲノムDNAの配列を決定し、由来するヒトにより異なるゲノムの部分の配列を決定することは当業者が容易になし得ることである。そして、請求項1に係る発明のポリヌクレオチドが上記周知技術から予測できない有利な効果を有するものとも認められない。
2.実施可能要件について
物の発明についての実施できるとは、その物をつくることができ、かつ、その物を使用できることである。
発明の詳細な説明には、請求項1に係る発明のポリヌクレオチドは法医学的鑑定に使用できることが記載されているが、通常単独のSNPを法医学的鑑定に用いることはないので、法医学的鑑定に使用できることを記載したのみでは、本願発明のSNPを有するポリヌクレオチドが上記「使用できること」に該当することを示したことにはならない。
拒絶理由に対する対処
通常、上記拒絶理由2を解消することはできない。
 6.5 進歩性があり、かつ、実施可能要件が満たされる場合
6.5 進歩性があり、かつ、実施可能要件が満たされる場合
事例7 DNA断片
特許請求の範囲
【請求項1】
配列番号16で表されるDNA配列からなるポリヌクレオチド
発明の詳細な説明の概要
このポリヌクレオチドは、疾病Yの患者の肝細胞から構築されたcDNAライブラリーで見出されるが、健常人の肝細胞においては検出されない、長さ500bpのcDNAの一つである。
ノーザンハイブリダイゼーションにより、対応するmRNAは疾病Yの患者の肝細胞においてのみ発現されていることが確認された。したがって、このポリヌクレオチドは疾病Yを診断に用いることができる。
先行技術調査の結果
疾病Yの患者に特有のポリヌクレオチド及びタンパク質は知られていない。
相同性が30%以上のDNA及びアミノ酸配列は発見されなかった。
拒絶理由の概要
なし。
(補足説明)
1.請求項1に係る発明のポリヌクレオチドは、疾病Yの診断に利用できるという、従来技術から予測できない顕著な効果を有する。
2.請求項1が「配列番号16で表されるDNA配列を含むポリヌクレオチド」と記載されていた場合。
請求項1に係る発明には、配列番号16で表されるDNA配列からなるポリヌクレオチドを一部分として含む、あらゆるポリヌクレオチドが含まれることになる。非常に長い非特徴的な部分を有するポリヌクレオチドの中には、疾病Yの診断に使用できないものが包含されると解されるから、請求項1に係る発明は実施不可能な部分を含んでいるという拒絶理由が通知される。(この拒絶理由は、配列番号6で表されるDNA配列からなるポリヌクレオチドにDNAが付加されたポリヌクレオチドは全て、診断用プローブとして使用できないという意図で通知されるものではない。)
事例8 全長cDNA
特許請求の範囲
【請求項1】
配列番号17で表されるDNA配列からなるポリヌクレオチド
発明の詳細な説明の概要
配列番号17で表されるDNA配列からなるポリヌクレオチドは、ヒト肝細胞cDNAライブラリーから取得された、2700個の塩基からなるcDNAである。また、該ポリヌクレオチドは、配列番号18で表される900個のアミノ酸配列からなるポリペプチドをコードするものである。
そして、実際に発現させ、該ポリペプチドはヒトのYY1因子であることを確認した。
先行技術調査の結果
相同性が80%以上のDNA及びアミノ酸配列、並びに、YY1因子に関する先行技術は発見されなかった。
拒絶理由の概要
なし。
(補足説明)
YY1因子の特定の機能、すなわち技術的に意味のある特定の用途が推認できる機能は知られている。
事例9 SNP
特許請求の範囲
【請求項1】
配列番号19で表されるDNA配列からなるポリヌクレオチド(位置50番目はg)において、50番目の塩基を含む20~100の連続したDNA配列からなるポリヌクレオチド
発明の詳細な説明の概要
配列番号19で表されるDNA配列(長さ500塩基)において、50番目のgがcであるDNA配列からなるポリヌクレオチドは知られていた。
配列番号19で表されるDNAにおける50番目の塩基が多型部位であることが示され、そして配列番号19で表されるDNA配列からなるポリヌクレオチドにおいて、50番目の塩基(g)を含む20~100の連続したDNA配列からなるポリヌクレオチドは、Z病の診断薬として利用できることが実験的に示されている。
先行技術調査の結果
配列番号19で表されるDNA配列からなるポリヌクレオチドは知られていない。また、請求項1に係る発明のポリヌクレオチドも知られていない。さらに、50番目の塩基の多型性とZ病との関連は知られていない。50番目がcであるDNA配列が構造遺伝子の一部であることが分かっているが、その遺伝子がコードするタンパク質とZ病との関係は知られていない。
拒絶理由の概要
なし。
(補足説明)
請求項1に係る発明のポリヌクレオチドは、Z病の診断薬として利用できるという顕著な効果を有する。
 7. タンパク質立体構造関連発明事例集
7. タンパク質立体構造関連発明事例集
 7.1 発明について
7.1 発明について
事例1 (「発明」に該当しない場合) 立体構造座標データ
特許請求の範囲
【請求項1】
図1で記載された原子座標によって生成されたタンパク質Pのコンピュータモデル。
【請求項2】
タンパク質モデリングアルゴリズムに基づいて動作するときタンパク質Pの三次元構造を生じる図1で示されたタンパク質Pの原子座標を含むデータ配列。
【請求項3】
図1に示すタンパク質Pの原子座標を記録した、コンピュータ読み取り可能な記録媒体。
発明の詳細な説明の概要
新たに作成されたタンパク質Pの結晶に対してX線結晶構造解析を行い、図1で記載された原子座標を含むデータ配列を得た。当該タンパク質Pが活性化することにより血圧が下がることについての実験データ及びその説明は実施例に示している。出願時点において原子座標データからタンパク質モデルを作成するアルゴリズムは周知技術である。図1に示したタンパク質Pの原子座標はin silico(コンピュータにより補助された)スクリーニング方法に有用である。
拒絶理由の概要
情報の提示それ自体、提示手段や提示方法に技術的特徴を有さないような、単なる情報の提示(提示される情報の内容にのみ技術的特徴を有するものであって、情報の提示を主たる目的とするもの)は特許法第29条第1項柱書 でいう「発明」(「自然法則を利用した技術思想の創作」)に該当しない。
でいう「発明」(「自然法則を利用した技術思想の創作」)に該当しない。
当該請求項1に係るコンピュータモデル、請求項2に係るデータ配列、請求項3に係る当該データ配列を格納したコンピュータ読み取り可能な記録媒体はいずれも情報の単なる提示であり、提示それ自体か提示手段や提示方法に技術的特徴があるような情報の提示ではない。
したがって、請求項1-3に係る発明はいずれも「発明」に該当しない。
事例2 (「発明」に該当しない場合) ファーマコフォア
特許請求の範囲
【請求項1】
下記式により定義される、分子中の原子の空間的配置を有するファーマコフォア:
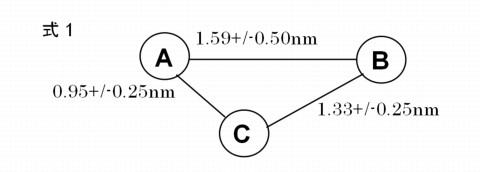
ここでA及びBはいずれも電子供与基を表し、Cは疎水性基の一部を構成する炭素原子を表し、距離はそれぞれの原子の中心間距離を表す。
発明の詳細な説明の概要
本出願におけるファーマコフォアとは、望ましい生物学的活性を担うと考えられる化学要素(例えば、疎水性基、荷電/イオン性基、水素結合供与基/受容基、分子基本骨格)の空間配置についての情報特有の表現で表わされた分子の特徴の包括的概念を表現したものである。タンパク質Pは従来公知のタンパク質であり、そのアミノ酸配列も従来公知である。タンパク質Pの活性化により血圧が下がることは、従来公知であった。【式1】で示されるファーマコフォアは、タンパク質Pのリガンド結合ポケットの構造が通常の方法を用いて推定されたタンパク質Pのリガンド結合ポケットの立体構造から判断されたものである。ファーマコフォアに基づいて新規のリガンドが設計され、当該リガンドが比較的高い親和性をもってタンパク質に結合することができる。
拒絶理由の概要
ファーマコフォアの技術的特徴は情報の内容にのみ存在しており、ファーマコフォアそのものは情報の単なる提示にすぎない。
したがって、この請求項に係る発明は「発明」に該当しない。
(補足説明)
事例1を参照のこと。
事例3 (「発明」に該当しない場合) 立体構造座標データを用いたコンピュータスクリーニング方法並びに当該方法により同定された化合物の名称及び構造を含む情報を記録したデータベース
特許請求の範囲
【請求項1】
タンパク質Pに結合可能な化合物を同定する方法であって、タンパク質Pの結合ポケットの空間座標を決定するために、三次元分子モデリングアルゴリズムを図1に示されたタンパク質Pの原子座標に用いる工程、タンパク質Pの結合ポケットの空間座標に対して、保存されている候補化合物のセットの空間座標を、コンピュータ上でスクリーニングする工程を含む方法。
【請求項2】
請求項1の方法により同定された化合物の名称及び構造を含む情報を記録したデータベース。
発明の詳細な説明の概要
タンパク質Pは従来公知のタンパク質であり、そのアミノ酸配列や、タンパク質Pの活性化により血圧が下がることについても、公知であった。タンパク質Pの原子座標(リガンドが結合していないタンパク質自身の生データ)は図1に示されているが、結合ポケットの位置は不明である。タンパク質の結合ポケットを予測するプログラム(結合に関与するアミノ酸残基を比較的多数出力するものである。)についての一般的な情報が開示されており、また常用されるin silicoスクリーニング用プログラムについて一般的な情報も開示している。また、ペプチドモデリングと推論的な薬物設計による結合の方法はこの技術分野において周知の事実である。結合ポケット予測プログラム及びin silicoスクリーニング用プログラムを使用することによって、当業者が当該タンパク質に結合する化合物を同定できる。(明細書には、タンパク質Pの原子座標を用いて化合物を同定したことについての実施例は記載されていない。)
拒絶理由の概要
「自然法則を利用した技術的思想の創作」であるためには、請求項に係る発明が一定の目的を達成できる具体的なものでなければならない。(平成9年(行ケ)第206号(東京高判平成11年5月26日判決言渡))請求項1に係る発明は、化合物を対象として何らかの処理を具体的に行うものではなく、また、請求項に係る発明をソフトウェア関連発明として考慮した場合においても、ソフトウェアによる情報処理とハードウェア資源とがどのように協働しているか具体的に記載されておらず、当該発明は「自然法則を利用した技術的思想の創作」に該当しないと判断される。
請求項2に係る発明は、化合物の名称及び構造を含む情報を記録したデータベースであって、提示される情報の内容のみに特徴を有するものである。
したがって、請求項1及び請求項2に係る発明はいずれも「発明」に該当しない。
 7.2 新規性について
7.2 新規性について
事例4 (新規性が満たされない場合) 立体構造により特定された公知タンパク質
特許請求の範囲
【請求項1】
図1に記載した原子座標によって定義された構造を有する単離精製されたタンパク質。
発明の詳細な説明の概要
アミノ酸側鎖の座標を含むタンパク質Pの立体構造を図1に示す。また、タンパク質Pの由来する生物名はXであり、分子量はYである。タンパク質Pの投与により血圧が低下し、そのことは実施例の中で証明している。構造座標は0.2nmの解像度でNMRによって溶液状のタンパク質から得られたものである。
先行技術調査の結果
タンパク質Pの立体構造を開示し、あるいは示唆する先行技術は発見されなかった。先行技術は同じ生物に由来し、同じ特定機能を有し、かつほぼ同様の分子量を有する単離精製されたタンパク質を開示している。
拒絶理由の概要
先行技術が同じ生物に由来し、同じ特定機能を有し、かつほぼ同様の分子量を有するタンパク質を開示しており、開示されているタンパク質は一般的に溶液状態で存在したものと見なされるので、引用文献に記載されたタンパク質の立体構造を同様の手法を用いて評価すれば、図1に示される立体構造となる蓋然性が高い。よって、請求項の溶液状態のタンパク質が先行技術のタンパク質と同一であるとする一応の合理的な疑いが成り立つ。
(補足説明)
一方、出願人が請求項のタンパク質が先行技術のタンパク質とは異なるものであるという根拠を十分示すことができれば、拒絶理由は解消する。
事例5 (新規性が満たされない場合)立体構造座標データを用いたコンピュータスクリーニング方法
特許請求の範囲
【請求項1】
候補化合物の立体構造を図5に示された立体分子モデルと対比することによって、タンパク質Pに結合する化合物を同定する方法であって、次のステップを含む方法:
- (1)
...
- (2)
...
(..)...
(n)...
(図5の立体分子モデルは、タンパク質Pの結合ポケットを構成するアミノ酸(すなわち、アミノ酸223、224、227、295、343、366、370、378及び384)に含まれ、候補化合物の水素結合性官能基と水素結合を形成することができるヘテロ原子の位置を示すものである。
ステップ(1)から(n)は
a) 図5に示された三次元分子モデルの座標データはタンパク質Pの原子間距離が容易に検索可能なようなデータ構造へ入力され、
b) 三次元分子モデルにおいて結合ポケットを形成するヘテロ原子と、異なる候補化合物の水素結合性官能基の間の距離が比較され、その結果、その2つの構造間の最適な水素結合に基づいたタンパク質Pの結合ポケットの三次元分子モデルによる、最も安定な複合体を理論的に構成する候補化合物の同定を可能とする、データ処理方法である。)
発明の詳細な説明の概要
タンパク質Pは従来公知のタンパク質であり、そのアミノ酸配列も従来公知であった。タンパク質Pの投与により血圧の低下が生じることも、従来公知であった。タンパク質Pと天然のリガンドとの共結晶状態における原子座標をX線結晶構造解析の結果として示す。タンパク質Pの結合ポケットの活性アミノ酸残基がアミノ酸223、224、227、295、343、366、370、378及び384ということが結論づけられる。どのように図5の立体分子モデルがタンパク質Pの結合ポケットの三次元構造を含むかについても示す。請求された同定方法についての実施例によっていくつかの化合物が同定されている。同定された化合物の実際の結合親和性について、実験データとして示す。示されたデータに基づき、請求項の方法によって、何らかの生物活性が期待できる程度にタンパク質Pに強く結合しうるいくつかの化合物を実際に同定できることが予想される。
先行技術調査の結果
タンパク質Pの結合部位を示唆する先行技術は発見されなかった。関心あるタンパク質の結合ポケットの立体分子モデルと候補化合物の立体構造とを比較するin silicoスクリーニング用プログラム及び、原子間距離を最適化する座標データの格納方法は先行技術に記載されている。先行技術に開示された化合物の同定方法と本願請求項1に記載された化合物の同定方法の違いは、用いる立体分子モデルがタンパク質Pの立体構造に基づく図5に示されたものでなく、別の立体構造解析データに基づくモデルによるものであることのみである。
拒絶理由の概要
請求項に係る発明は情報処理のためのコンピュータ・ソフトウェア関連発明であり、その技術的特徴は用いられる情報処理方法である。情報処理方法において、情報処理の手順が先行技術のものと相違しない場合、新規性は肯定されない。
本事例において、先行技術と当該発明の相違点として挙げられる「図5に示された立体分子モデル」という事項は、データの内容に言及しているに過ぎず、コンピュータの情報処理の手順を変更するものではないので、この相違点をもって本願請求項に係る発明の新規性は肯定されない。
事例6 (新規性、進歩性があり、かつ実施可能要件が満たされる場合) タンパク質の結晶
特許請求の範囲
【請求項1】
タンパク質Pの結晶であって、単位格子定数がa=4.0nm,b=7.8nm,及びc=11.0nmである、上記結晶。
発明の詳細な説明の概要
タンパク質Pのアミノ酸配列は公知であった。タンパク質Pの投与により血圧の低下が生じることも、従来公知であった。本願発明者は、タンパク質Pの安定な結晶を新規に製造することに成功した。結晶の製造方法については明細書中の説明及び実験データに示したとおりである。結晶状態のタンパク質Pは不活性であるが、結晶を溶液に溶解することによって、再び活性を持つようになることについても実験データとして示している。タンパク質の結晶化に用いられる通常の先行技術は、このタンパク質Pには適用できないことも実験データで示されており、クレームされたタンパク質Pの結晶の製造には技術的困難が存在したことは明らかである。
先行技術調査の結果
タンパク質Pあるいは関連するタンパク質の結晶を開示又は示唆する先行技術文献は発見されなかった。また、タンパク質Pの結晶化方法に関する先行技術はなかった。
拒絶理由の概要
なし。
(補足説明)
タンパク質結晶はタンパク質そのもの(物質)とはその形状、構造が異なり区別できるので、新規性がある。先行技術はタンパク質Pの結晶、あるいは請求項に記載のタンパク質Pの結晶の製造方法を何ら教示するものでなく、さらにタンパク質の結晶化に用いられる公知の方法ではタンパク質Pの結晶化が不成功に終わっているので、結晶に係る発明は進歩性を満たす。
事例7 (新規性、進歩性があり、かつ実施可能要件が満たされる場合)有意に高い活性を有するタンパク質の部分ポリペプチド
特許請求の範囲
【請求項1】
配列番号1に示されたタンパク質Pのアミノ酸214から218のうち一つで始まり、アミノ酸394から401のうち一つで終わる、タンパク質Pの部分からなる単離精製されたポリペプチド。
発明の詳細な説明の概要
タンパク質Pは従来公知のタンパク質であり、そのアミノ酸配列も従来公知であった。タンパク質Pの投与により血圧の低下が生じることも、従来公知であった。発明者らは、タンパク質Pの結合ポケットの活性残基がアミノ酸223、224、227、295、343、366、370、378及び384からなることを、新規に発見した。配列番号1のアミノ酸214から218のいずれかのアミノ酸によって始まり、また、アミノ酸394から401のいずれかのアミノ酸によって終わる全てのペプチドは、タンパク質Pの活性な結合ポケットへと折り畳まれることができるタンパク質ドメインであることをX線結晶回折データによって確認した。タンパク質Pの天然リガンドにより活性化された場合、上記ドメイン単独の方が全長のタンパク質よりも有意に強いシグナル活性を有することを証明した。
先行技術調査の結果
タンパク質Pの結合部位を示唆する先行技術は発見されなかった。当該結合ポケットを含むタンパク質構造ドメインを示唆する先行技術も発見されなかった。
拒絶理由の概要
なし。
(補足説明)
当該ポリペプチドは全長タンパク質そのもの(物質)とは区別できるので、新規性がある。先行技術はタンパク質Pの特定の部位からなるポリペプチド、あるいはポリペプチドの部位特定方法を何ら教示するものでなく、当該ポリペプチドはタンパク質の全長のタンパク質よりも有意に強い活性を有するので進歩性を満たす。
 7.3 実施可能要件及び明確性について
7.3 実施可能要件及び明確性について
事例8 (実施可能要件及び明確性が満たされない場合) 有意に高い活性を有するタンパク質の部分ポリペプチド
特許請求の範囲
【請求項1】
図1に示されたアミノ酸223、224、227、295、343、366、370、378及び384の構造座標により定義された、単離精製されたタンパク質Pの結合ポケットを含む分子。
発明の詳細な説明の概要
タンパク質Pは従来公知のタンパク質であり、そのアミノ酸配列も従来公知であった。タンパク質Pの投与により血圧の低下が生じることも、従来公知であった。発明者らは、タンパク質Pの結合ポケットの活性残基がアミノ酸223、224、227、295、343、366、370、378及び384からなることを、新規に発見した。配列番号1のアミノ酸214から218のいずれかのアミノ酸によって始まり、また、アミノ酸394から401のいずれかのアミノ酸によって終わる全てのペプチドは、タンパク質Pの活性な結合ポケットへと折り畳まれることができるタンパク質ドメインであることをX線結晶回折データによって確認した。タンパク質Pの天然リガンドにより活性化された場合、上記ドメイン単独の方が全長のタンパク質よりも有意に強いシグナル活性を有することを証明した。
拒絶理由の概要
「結合ポケット」は全長タンパク質又は完全な構造ドメインでなければ正しい立体構造にはフォールドしない(つまり、正しい立体構造にフォールドする構造ドメインを得るためには、アミノ酸配列を正しい位置で「切る」必要がある)。
したがって、当該請求項における特定のアミノ酸の集合に対応した現実の化合物を製造することは明細書の記載からは不可能であり、請求項に係る発明には実施可能でない部分が含まれている。
また、結合ポケットとして特定されたアミノ酸以外の「分子」として存在するための具体的な構造が明らかでないため、請求項に係る発明は明確でない。
(補足説明)
公知のタンパク質Pは当該請求項の結合ポケット部位を包含する化合物であって、区別することができないので、請求項に係る発明はタンパク質Pを開示する公知技術と同一でもある。
事例9 (実施可能要件及び明確性が満たされない場合) コンピュータスクリーニング方法によって同定された化合物
特許請求の範囲
【請求項1】
候補化合物の立体構造を図5に示された立体分子モデルと対比することによって、タンパク質Pに結合する化合物を同定する方法によって同定される化合物であって、同定方法が次のステップを含むもの:
- (1)
...
- (2)
...
(..)...
(n) ...
(図5の立体分子モデルは、タンパク質Pの結合ポケットを構成するアミノ酸(すなわち、アミノ酸223、224、227、295、343、366、370、378及び384)に含まれ、候補化合物の水素結合性官能基と水素結合を形成することができるヘテロ原子の位置を示すものである。
ステップ(1)から(n)は
a) 図5に示された三次元分子モデルの座標データはタンパク質Pの原子間距離が容易に検索可能なようなデータ構造へ入力され、
b) 三次元分子モデルにおいて結合ポケットを形成するヘテロ原子と、異なる候補化合物の水素結合性官能基の間の距離が比較され、その結果、その2つの構造間の最適な水素結合に基づいたタンパク質Pの結合ポケットの三次元分子モデルによる、最も安定な複合体を理論的に構成する候補化合物の同定を可能とする、データ処理方法である。)
発明の詳細な説明の概要
タンパク質Pは従来公知のタンパク質であり、そのアミノ酸配列も従来公知であった。タンパク質Pの投与により血圧の低下が生じることも、従来公知であった。タンパク質Pと天然のリガンドとの共結晶状態における原子座標をX線結晶構造解析の結果として示す。タンパク質Pの結合ポケットの活性アミノ酸残基がアミノ酸223、224、227、295、343、366、370、378及び384ということが結論づけられる。どのように図5の立体分子モデルがタンパク質Pの結合ポケットの三次元構造を含むかについても示す。請求された同定方法についての実施例によっていくつかの化合物が同定されている。同定された化合物の実際の結合親和性について、実験データとして示す。示されたデータに基づき、請求項の方法によって、何らかの生物活性が期待できる程度にタンパク質Pに強く結合しうるいくつかの化合物を実際に同定できることが予想される。
拒絶理由の概要
特定の化学構造を有する化合物を得るための実施例又はその手掛かりとなる開示が明細書中に存在しないので、そのような化合物を具体的に想起することは困難であり、発明を実施するために無数の化合物を製造、スクリーニングすることは当業者に期待しうる程度を超える試行錯誤を要するものである。よって、実施可能要件を満たさない。
また、コンピュータスクリーニング方法のみで規定された化合物が具体的にどのようなものであるかを理解することは困難であることが出願時の技術常識である。したがって、かかる技術常識を考慮すると、化学構造等が何ら規定されず、上記スクリーニング方法のみで規定された「化合物」は、技術的に十分に特定されていないことが明らかであり、明細書及び図面の記載を考慮しても、請求項の記載から発明を明確に把握することができない。
事例10 (実施可能要件及び明確性が満たされない場合) ファーマコフォアで定義された化合物
特許請求の範囲
【請求項1】
下記式により定義される、分子中の原子の空間的配置を有するファーマコフォアで定義された単離された化合物又はその塩。
ここでA及びBはいずれも電子供与基を表し、Cは疎水性基の一部を構成する炭素原子を表し、距離はそれぞれの原子の中心間距離を表す。
発明の詳細な説明の概要
本出願におけるファーマコフォアとは、望ましい生物学的活性を担うと考えられる化学要素(例えば、疎水性基、荷電/イオン性基、水素結合供与基/受容基、分子基本骨格)の空間配置についての情報特有の表現で表された分子の特徴の包括的概念を表現したものである。タンパク質Pは従来公知のタンパク質であり、そのアミノ酸配列も従来公知である。タンパク質Pの活性化により血圧が下がることは、従来公知であった。【式1】で示されるファーマコフォアは、タンパク質Pのリガンド結合ポケットの構造が通常の方法を用いて推定されたタンパク質Pのリガンド結合ポケットの立体構造から判断されたものである。ファーマコフォアに基づいて新規のリガンドが設計され、当該リガンドが比較的高い親和性をもってタンパク質に結合することができる。
拒絶理由の概要
式1はわずか3つの原子の性質と位置を定義するにすぎないため、実施例に示された1つのリガンド以外に当該定義のリガンド構造を当業者が想定することは困難であり、そのような化合物を製造、スクリーニングすることも当業者に期待しうる程度を超える試行錯誤を要する。したがって、請求項に係る発明は実施可能要件を満たさない。
また、わずか 3 つの原子の性質や位置が規定されたのみでは、そのような規定を満たすリガンド構造を理解することは困難であることが出願時の技術常識である。したがって、かかる技術常識を考慮すると、化学構造等が何ら規定されず、わずか 3 つの原子の性質と位置のみで規定された「化合物」は、技術的に十分に特定されていないことが明らかであり、明細書及び図面の記載を考慮しても、請求項の記載から発明を明確に把握することができない。
 8. 微生物等の寄託の要否に関する事例集
8. 微生物等の寄託の要否に関する事例集
以下においては、出願前に微生物等(ここにおいて「微生物等」には、微生物、植物、動物が含まれる。) を寄託する必要があるか否かの判断に関して、具体的な事例に基づいて説明する。
寄託の要否に関する一般的な事項については「5. 寄託」参照。
本事例集には、以下の事例が含まれている。
8.1 細菌に関する発明
事例1-1 当業者が細菌を容易に入手できる事例(寄託不要)
事例1-2 当業者が細菌を容易に入手できない事例(寄託必要)
事例1-3 細菌由来のDNAに係る発明の事例(寄託不要)
8.2 抗体に関する発明
事例2-1 明細書の記載に基づいて当業者がハイブリドーマを製造しうる事例(寄託不要)
事例2-2 明細書の記載に基づいて当業者がハイブリドーマを製造しうる事例(寄託不要)
事例2-3 当業者がハイブリドーマを容易に入手できない事例(寄託必要)
8.3 細胞に関する発明
事例3-1 明細書の記載に基づいて当業者が細胞を製造しうる事例(寄託不要)
事例3-2 当業者が細胞を容易に入手できない事例(寄託必要)
8.4 動物に関する発明
事例4-1 明細書の記載に基づいて当業者が動物を製造しうる事例(寄託不要)
事例4-2 当業者が動物を容易に入手できない事例(寄託必要)
(留意事項)
本事例集は、各事例において、新規性・進歩性の欠如等の拒絶理由がないことを意味するものではない。
 8.1 細菌に関する発明
8.1 細菌に関する発明
事例1-1 当業者が細菌を容易に入手できる事例(寄託不要)
特許請求の範囲
【請求項1】
ストレプトマイセス・リビダンス xyz-1株(Streptomyces lividans xyz-1;ATCC ******)由来であって、下記の理化学的性質を有するβ-ガラクトシダーゼ。
(a) 作用および基質特異性:β-D-ガラクトシド結合を有する基質を加水分解し、D-ガラクトース基を遊離する。
(b) 至適pH:4.5
(c) 安定pH:3.0~5.5
(d) 至適温度:55℃
(e) 安定温度:50℃
(f) 分子量:ゲル濾過法による測定で200kDである。
発明の詳細な説明の概要
β-ガラクトシダーゼによる加工の対象として、牛乳、チーズホエー、乳糖液等の中性~酸性の原料が想定されるため、酸性領域で十分な酵素活性を有するβ-ガラクトシダーゼが望まれていたが、酸性領域で十分な酵素活性を有するβ-ガラクトシダーゼを産生する微生物は出願時まで知られていなかった。
発明者らは、ストレプトマイセス・リビダンス xyz-1株から、請求項1に係るβ-ガラクトシダーゼを特定の手法を用いることにより単離した。また、該ストレプトマイセス・リビダンス xyz-1株は、ATCCが発行するカタログに保存番号ATCC ******として掲載されており、出願前に自由に分譲されうるものであった。
[微生物等の寄託の要否に関する説明]
本事例においては、発明の詳細な説明の記載からみて、ストレプトマイセス・リビダンス xyz-1株は、信用できる保存機関であるATCCに保存され、ATCCの発行するカタログにより自由に分譲されうることが出願前に明らかな微生物である。また、発明の詳細な説明には、ストレプトマイセス・リビダンス xyz-1株の保存番号も記載されている。
したがって、ストレプトマイセス・リビダンス xyz-1株は当業者が容易に入手することができる微生物であり、当業者であれば明細書に記載の特定の手法を用いて請求項1に係るβ-ガラクトシダーゼを単離することができる。
よって、ストレプトマイセス・リビダンス xyz-1株を寄託する必要はない。
事例1-2 当業者が細菌を容易に入手できない事例(寄託必要)
特許請求の範囲
【請求項1】
ダイオキシン分解能を有する、バチルス ズブチルス(Bacillus subtilis)T-169株。
発明の詳細な説明の概要
富山湾の海底泥を試料として採取し、当該試料から当業者に周知の方法でバチルス ズブチルス T-169株を単離した。該バチルス ズブチルス T-169株の分類学的性質を詳細に分析し、同種内の公知の菌株との相違点を検討したところ、該バチルス ズブチルス T-169株は新菌株であることが判明した。また、実験を行うことにより、該バチルス ズブチルス T-169株がダイオキシンを高効率で分解できることが明らかとなった。
[微生物等の寄託の要否に関する説明]
通常、土壌や海水などに存在する微生物の種類や量は、その土壌や海水が特定の地域から得られたものであっても、必ずしも一定であるとは限らない。
したがって、特定の地域の土壌や海水などから採取した試料を用いて新規な微生物を単離した場合でも、該土壌や海水などから再度採取した試料の中に、該新規な微生物が存在することの合理的な根拠がない限り、該新規な微生物を再現性をもって取得することは困難である。
本事例においては、発明の詳細な説明に、富山湾の海底泥から再度採取した試料の中に、バチルス ズブチルス T-169株が存在することの合理的な根拠が記載されていない。
してみると、当業者が追試をした時に、再現性をもってバチルス ズブチルス T-169株を取得することはできないので、バチルス ズブチルス T-169株は明細書の記載に基づいて当業者が製造しうる微生物ではない。
よって、バチルス ズブチルス T-169株は当業者が容易に入手することができる微生物ではないので、バチルス ズブチルス T-169株を寄託する必要がある。
事例1-3 細菌由来のDNAに係る発明の事例 (寄託不要)
特許請求の範囲
【請求項1】
コリネ型細菌K-336株由来のアルギノコハク酸シンターゼをコードし、配列番号1で表される塩基配列を含むDNA。
【請求項2】
請求項1記載のDNAを含む発現ベクター。
【請求項3】
請求項2記載のベクターを発現可能に保持する、形質転換体。
発明の詳細な説明の概要
薬剤耐性に基づき土壌から単離した、L-アルギニンを産生するコリネ型細菌K-336株の分類学的性質を詳細に分析し、在来の類似種との異同を検討したところ、該コリネ型細菌K-336株は新種であることが判明した。
コリネ型細菌におけるL-アルギニン生合成経路にはArgAからArgHまでの遺伝子が関与することは出願時に公知であった。発明者らは、コリネ型細菌K-336株から、配列番号1で表される塩基配列を含むArgG遺伝子を初めて単離精製し、ArgG遺伝子を周知の遺伝子工学的手法で発現させ、ArgG遺伝子がコードするタンパク質がアルギノコハク酸シンターゼであることを確認した。
[微生物等の寄託の要否に関する説明]
本事例においては、請求項1に係る発明はDNAに係るものであって、コリネ型細菌K-336株に係るものではない。そして、当該DNAの塩基配列は明細書に具体的に記載されているから、当業者はこの塩基配列に基づき、人工合成方法等を通じて当該DNAを取得することができる。また、当業者であれば、当該DNAを適切な発現ベクターに組み込んで、当該発現ベクターを発現可能に保持する形質転換体を製造することができる。
よって、コリネ型細菌K-336株を寄託する必要はない。
 8.2 抗体に関する発明
8.2 抗体に関する発明
事例2-1 明細書の記載に基づいて当業者がハイブリドーマを製造しうる事例(寄託不要)
特許請求の範囲
【請求項1】
配列番号1で表されるアミノ酸配列からなる抗原タンパク質A。
【請求項2】
請求項1に記載の抗原タンパク質Aに対するモノクローナル抗体。
【請求項3】
請求項2に記載のモノクローナル抗体を産生するハイブリドーマ。
発明の詳細な説明の概要
ウイルスXの外膜から新規な抗原タンパク質Aを単離精製したところ、抗原タンパク質Aは、ウイルスX感染
者由来の血清のみと反応したことから、抗原タンパク質AはウイルスX感染者の同定に有用である。また、抗原タンパク質Aの部分アミノ酸配列を決定し、該部分アミノ酸配列に基づいて周知の遺伝子工学的手法により、配列番号1で表されるアミノ酸配列からなる抗原タンパク質Aをコードする遺伝子をクローニングした。
(注)抗原タンパク質Aに対して特異的に反応するモノクローナル抗体を製造した実施例はない。
[微生物等の寄託の要否に関する説明]
本事例において、請求項2に係るモノクローナル抗体は、抗原のみで特定されたモノクローナル抗体である。
一般に、免疫原性を有するタンパク質が得られた際に、該タンパク質を免疫原として周知のハイブリドーマ法により、該タンパク質に対するモノクローナル抗体を得ることができるとの技術常識がある。
そして、当業者であれば、発明の詳細な説明の記載に基づいて、抗原タンパク質Aをコードする遺伝子を取得し、周知の遺伝子工学的手法を用いて該遺伝子を発現させ、配列番号1で表されるアミノ酸配列からなる抗原タンパク質Aを製造することができる。また、該抗原タンパク質Aが免疫原性を有することは明らかである。
してみれば、当業者であれば、発明の詳細な説明の記載に基づいて、抗原タンパク質Aを製造し、該抗原タンパク質Aを免疫原として、周知のハイブリドーマ法により、請求項2に係るモノクローナル抗体とそれを産生するハイブリドーマを取得することができる。
したがって、請求項3に係るハイブリドーマは明細書の記載に基づいて当業者が製造しうる微生物である。
よって、請求項3に係るハイブリドーマは当業者が容易に入手することができる微生物であるので、請求項3に係るハイブリドーマを寄託する必要はない。
事例2-2 明細書の記載に基づいて当業者がハイブリドーマを製造しうる事例 (寄託不要)
特許請求の範囲
【請求項1】
ウイルスYの表面抗原Pに対して結合定数:1010M-1以上で反応することを特徴とする、IgM型モノクローナル抗体。
【請求項2】
請求項1に記載のモノクローナル抗体を産生するハイブリドーマ。
発明の詳細な説明の概要
ウイルスYの表面抗原Pは既に単離精製され、それを検出できる抗体も出願時に公知であった。しかしながら、IgM型モノクローナル抗体は、凝集しやすい性質等のために、検出にはあまり望ましくないと考えられていたところ、発明者らは、IgM型モノクローナル抗体であって、高感度にウイルスYの表面抗原Pを検出できるものを初めて取得した。
発明者らは、該表面抗原Pをコードするアミノ酸配列から、ある特定の部分アミノ酸配列を選択して、該特定の部分アミノ酸配列からなるポリペプチドを製造し、該ポリペプチドが免疫原として機能することを確認した。そして、該ポリペプチドを用いて、周知のハイブリドーマ法に基づきモノクローナル抗体を産生するハイブリドーマを製造した。その結果、抗体産生が確認できるハイブリドーマが149株得られた。そのうち、10株を選択し、該選択したハイブリドーマが産生する抗体の結合定数を測定したところ、IgM型であって結合定数:1010M-1以上を満たす抗体を産生するハイブリドーマは3株しか確認できなかった。しかし、同様のハイブリドーマ製造実験を3回繰り返し実施したところ、いずれの場合においても、IgM型であって結合定数:1010M-1以上を満たす抗体を産生するハイブリドーマが少なくとも1株は取得された。
[微生物等の寄託の要否に関する説明]
本事例において、請求項1に係るモノクローナル抗体は、「ウイルスYの表面抗原Pに対して結合定数:1010M-1以上で反応する」という限定的な条件を満たすモノクローナル抗体である。
一般に、限定的な条件を満たすモノクローナル抗体を産生するハイブリドーマを取得することは、再現性がない場合が多いとの技術常識がある。
しかしながら、発明の詳細な説明には、ウイルスYの表面抗原Pをコードするアミノ酸配列から、ある特定の部分アミノ酸配列を選択することによって、「ウイルスYの表面抗原Pに対して結合定数:1010M-1以上で反応する」という限定的な条件を満たすIgM型モノクローナル抗体を産生するハイブリドーマを複数株取得することができたことが記載されている。さらに、該特定の部分アミノ酸配列からなるポリペプチドを免疫原として、同様のハイブリドーマ製造実験を繰り返し行うことにより、このような限定的な条件を満たすIgM型モノクローナル抗体を産生するハイブリドーマを、繰り返して取得することができたことが記載されている。
してみれば、当業者が追試をした時に、再現性をもって請求項1に係るモノクローナル抗体、及び、それを産生するハイブリドーマを取得することができる。
したがって、請求項2に係るハイブリドーマは明細書の記載に基づいて当業者が製造しうる微生物である。
よって、請求項2に係るハイブリドーマは当業者が容易に入手することができる微生物であるので、取得されたハイブリドーマを寄託する必要はない。
事例2-3 当業者がハイブリドーマを容易に入手できない事例(寄託必要)
特許請求の範囲
【請求項1】
受容体Zに結合して、細胞増殖を抑制することを特徴とする、モノクローナル抗体ABC-1。
【請求項2】
請求項1に記載の抗体を産生するハイブリドーマH-ABC-1。
発明の詳細な説明の概要
受容体Zは既に単離精製されており、受容体Zにアゴニストが結合することにより、細胞増殖が抑制されることは出願時に公知であった。また、受容体Zに結合して細胞増殖を抑制するモノクローナル抗体を製造する試みも出願時までになされていた。しかしながら、受容体Zに結合して細胞増殖を抑制する抗体は、出願時までに取得されていなかった。
発明者らは、受容体Zを免疫原として、周知のハイブリドーマ法に基づき、モノクローナル抗体を製造したところ、受容体Zに結合するモノクローナル抗体を産生するハイブリドーマは多数取得されたが、その中で細胞増殖を抑制するモノクローナル抗体を産生するハイブリドーマは1株のみであった。そして、該細胞増殖を抑制するモノクローナル抗体を「モノクローナル抗体ABC-1」と命名し、該「モノクローナル抗体ABC-1」を産生するハイブリドーマを「ハイブリドーマH-ABC-1」と命名した。
[微生物等の寄託の要否に関する説明]
本事例において、請求項1に係るモノクローナル抗体ABC-1は、ハイブリドーマH-ABC-1という特定の株のハイブリドーマにより産生されるモノクローナル抗体である。
一般に、特定の株のハイブリドーマを、周知のハイブリドーマ法により意図的に取得することは困難であるとの技術常識がある。
そして、発明の詳細な説明には、周知のハイブリドーマ法に基づき、モノクローナル抗体ABC-1を産生するハイブリドーマH-ABC-1が1株だけ取得されたことが記載されているのみであり、ハイブリドーマH-ABC-1を再現性をもって取得する方法について記載されていない。
したがって、当業者が追試をした時に、再現性をもって当該モノクローナル抗体ABC-1あるいはハイブリドーマH-ABC-1を取得することはできないので、ハイブリドーマH-ABC-1は明細書の記載に基づいて当業者が製造しうる微生物ではない。
よって、ハイブリドーマH-ABC-1は当業者が容易に入手することができる微生物ではないので、ハイブリドーマH-ABC-1を寄託する必要がある。
 8.3 細胞に関する発明
8.3 細胞に関する発明
事例3-1 明細書の記載に基づいて当業者が細胞を製造しうる事例(寄託不要)
特許請求の範囲
【請求項1】
マウス由来の肺癌細胞を含む不均一な細胞集団からマウス由来の肺癌細胞を分離する方法であって、
- (1)
配列番号1で表される塩基配列からなる肺癌細胞特異的プロモーターの支配下に、蛍光タンパク質をコードする核酸分子を連結したベクターを作製する工程、
- (2)
前記細胞集団に該ベクターを導入する工程、
- (3)
該細胞集団の中から蛍光を発する細胞としてマウス由来の肺癌細胞を同定し、分離する工程を含む方法。
【請求項2】
請求項1に記載の方法により分離された、マウス由来の肺癌細胞。
発明の詳細な説明の概要
肺癌細胞において特異的に機能する新規プロモーターをマウスからクローニングした。該プロモーターの塩基配列は配列番号1で表されるものである。また、周知技術に基づき、肺癌細胞を含む不均一な細胞集団をマウスより調製した。次に、該細胞集団に、該プロモーターの支配下に蛍光タンパク質の一種として周知であるGFPをコードする核酸分子を連結したベクターを導入することにより、該細胞集団内の肺癌細胞のみにおいてGFPを発現させ、該細胞集団の中から蛍光を発する細胞としてマウス由来の肺癌細胞を同定し分離した。
[微生物等の寄託の要否に関する説明]
本事例においては、発明の詳細な説明に、肺癌細胞で特異的に機能するプロモーターの塩基配列が具体的に記載されており、その支配下にGFPをコードする核酸分子を連結したベクターを用いて、不均一な細胞集団の中からマウス由来の肺癌細胞を同定・分離したことが記載されている。
してみれば、当業者が追試をした時に、再現性をもってマウス由来の肺癌細胞を同定・分離することができる。
したがって、請求項2に係るマウス由来の肺癌細胞は明細書の記載に基づいて当業者が製造しうる微生物である。
よって、請求項2に係るマウス由来の肺癌細胞は当業者が容易に入手することができる微生物であるので、同定・分離したマウス由来の肺癌細胞を寄託する必要はない。
事例3-2 当業者が細胞を容易に入手できない事例 (寄託必要)
特許請求の範囲
【請求項1】
マウス間葉系幹細胞に由来し、無血清培地で継代培養可能であって、該無血清培地で培養すると繊維状を呈し、目的とする細胞の馴化培地を含む培地で培養することにより、80%以上の割合で目的とする細胞に分化誘導される間葉系幹細胞H01株。
発明の詳細な説明の概要
マウス骨髄から取得した間葉系幹細胞を無血清培地で3週間培養し、死滅した細胞を除去した。その後、残存する細胞について継代を繰り返しながら分化能を検討したところ、アストロサイト馴化培地を含む培地で培養することによりアストロサイト様細胞に分化する突然変異細胞株が偶発的に得られた。そして、該突然変異細胞株を間葉系幹細胞H01株と命名した。ここで、該間葉系幹細胞H01株についてさらなる分化能の解析を行ったところ、脂肪細胞、平滑筋細胞、繊維芽細胞等の馴化培地を含む培地で培養することにより、ほぼ100%の割合でそれぞれの細胞へと分化誘導された。
[微生物等の寄託の要否に関する説明]
一般に、細胞の培養中に細胞のゲノムに生じる突然変異は、ランダムに生じるものであるので、特定の突然変異細胞株を、細胞培養中に意図的に取得することは困難であるとの技術常識がある。
本事例においては、発明の詳細な説明に、間葉系幹細胞H01株はマウス骨髄から取得した間葉系幹細胞を継代培養している過程で偶発的に得られた突然変異細胞株から樹立されたものであることが記載されているのみであり、間葉系幹細胞H01株を再現性をもって取得する方法について記載されていない。
したがって、当業者が追試をした時に、再現性をもって間葉系幹細胞H01株を取得することはできないので、間葉系幹細胞H01株は明細書の記載に基づいて当業者が製造しうる微生物ではない。
よって、間葉系幹細胞H01株は当業者が容易に入手することができる微生物ではないので、間葉系幹細胞H01株を寄託する必要がある。
 8.4 動物に関する発明
8.4 動物に関する発明
事例4-1 明細書の記載に基づいて当業者が動物を製造しうる事例(寄託不要)
特許請求の範囲
【請求項1】
配列番号1で表される塩基配列からなる原癌遺伝子を導入したトランスジェニックマウス。
発明の詳細な説明の概要
配列番号1で表される塩基配列からなる新規な原癌遺伝子をヒトからクローニングした。また、周知の遺伝子導入方法に基づいて、当該遺伝子を市販のBALB/c系マウス受精卵に導入し発生させることにより、複数のトランスジェニックマウスを作製したところ、それらは生後平均5ヶ月齢において腫瘍を発症した。
[微生物等の寄託の要否に関する説明]
本事例においては、発明の詳細な説明に、配列番号1で表される塩基配列からなる新規な原癌遺伝子が記載されており、市販のマウスを用いて、周知の遺伝子導入方法に基づいて、トランスジェニックマウスを作製したことが記載されている。
してみれば、当業者が追試をした時に、再現性をもって配列番号1で表される塩基配列からなる原癌遺伝子を導入したトランスジェニックマウスを作製することができる。
したがって、請求項1に係るトランスジェニックマウスは明細書の記載に基づいて当業者が製造しうる動物である。
よって、請求項1に係るトランスジェニックマウスは当業者が容易に入手することができる動物であるので、作製されたトランスジェニックマウス(その受精卵等)を寄託する必要はない。
事例4-2 当業者が動物を容易に入手できない事例(寄託必要)
特許請求の範囲
【請求項1】
初期病変として、生後3週齢で眼周囲に浮腫が認められるという特性を有する、皮膚炎を自然発症するRFGマウス。
発明の詳細な説明の概要
BALB/c系マウスを系統維持している過程において、初期病変として、生後3週齢で眼周囲に浮腫が認められ、清浄環境下で皮膚炎を自然発症する突然変異個体を偶発的に得た。その後、該突然変異個体から近交系を確立し、RFGマウスと命名した。近交系確立後、25世代を経る過程において、RFGマウスは初期病変として、生後3週齢で眼周囲に浮腫が認められるという特性を維持し、皮膚炎を自然発症した。
[微生物等の寄託の要否に関する説明]
一般に、マウスを系統維持している過程において、マウスのゲノムに生じる突然変異はランダムに生じるものであるので、特定の突然変異個体を、系統維持している過程において再現性をもって取得することは困難であるとの技術常識がある。
本事例においては、発明の詳細な説明に、RFGマウスは、BALB/c系マウスを系統維持している過程において偶発的に得られた突然変異個体から確立された近交系であることが記載されているのみであり、RFGマウスを再現性をもって取得する方法については記載されていない。
したがって、当業者が追試をした時に、再現性をもってRFGマウスを取得することはできないので、RFGマウスは明細書の記載に基づいて当業者が製造しうる動物ではない。
よって、RFGマウスは当業者が容易に入手することができる動物ではないので、RFGマウス(その受精卵等)を寄託する必要がある。

